
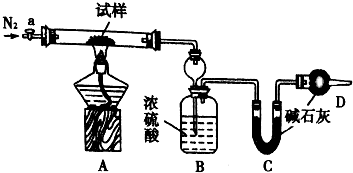
 小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m3、m5 |
分析 (1)小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),装置A中发生反应为碳酸氢钠受热分解生成碳酸钠、二氧化碳和水;碳酸钠晶体失水生成碳酸钠和水;
(2)装置B中的浓硫酸具有吸水性,可以吸收气体中的水蒸气;装置C中是碱石灰用来吸收碳酸氢钠分解生成的二氧化碳气体;
(3)实验过程中通入N2的目为把生成的水蒸气和二氧化碳气体全部赶到BC装置中完全吸收;
(4)由题意可知生成水的质量是(m4-m2)g,生成二氧化碳的质量为(m5-m3)g,原样品质量为m1g,可以利用生成的二氧化碳质量计算碳酸氢钠的质量,也可以由生成水的质量列方程组计算碳酸氢钠的质量,若再知道原样品质量即可计算碳酸氢钠的质量分数,所以利用ce组数据能计算,利用B组数据可以由生成二氧化碳的质量计算碳酸氢钠质量,再由生成水的质量计算得到碳酸钠晶体质量,进一步可以求碳酸氢钠质量分数;
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,可以利用二氧化碳质量计算,利用实验中所提供的数据得到准确的w(NaHCO3).
解答 解:(1)小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),装置A中发生反应为碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,反应的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;碳酸钠晶体失水生成碳酸钠和水,反应的化学方程式为:Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O;
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O;
(2)装置B中的浓硫酸具有吸水性,可以吸收气体中的水蒸气;装置C中是碱石灰用来吸收碳酸氢钠分解生成的二氧化碳气体;
故答案为:吸收反应生成的水蒸气;吸收反应生成的二氧化碳;
(3)实验过程中通入N2的目为把生成的水蒸气和二氧化碳气体全部赶到BC装置中完全吸收;
故答案为:使装置中的二氧化碳和水蒸气全部排出被装置BC全部吸收;
(4)由题意可知生成水的质量是(m4-m2)g,生成二氧化碳的质量为(m5-m3)g,原样品质量为m1g,可以利用生成的二氧化碳质量计算碳酸氢钠的质量,也可以由生成水的质量列方程组计算碳酸氢钠的质量,若再知道原样品质量即可计算碳酸氢钠的质量分数,所以利用ce组数据能计算,利用B组数据可以由生成二氧化碳的质量计算碳酸氢钠质量,再由生成水的质量计算得到碳酸钠晶体质量,进一步可以求碳酸氢钠质量分数;
故答案为:bce;
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,可以利用二氧化碳质量计算,利用实验中所提供的数据得到准确的w(NaHCO3)=$\frac{\frac{{m}_{5}-{m}_{3}}{44}×84}{{m}_{1}}$×100%=$\frac{42({m}_{5}-{m}_{3})}{11{m}_{1}}$×100%;
故答案为:$\frac{42({m}_{5}-{m}_{3})}{11{m}_{1}}$×100%.
点评 该题考查物质含量的测定,是高考中的常见题型,属于中等难度试题的考查.该题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和应试能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
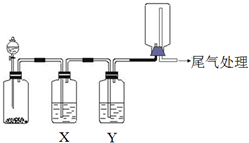
| 选项 | 实验目的 | X中试剂 | Y中 试剂 |
| A | 粗锌与稀盐酸制取 收集干燥的氢气 | 饱和食盐水 | 浓硫酸 |
| B | Na2SO3固体与较浓盐酸 反应制取收集干燥SO2 | 饱和Na2SO3溶液 | 浓硫酸 |
| C | 铜与稀硝酸制取并收集 纯净干燥的NO | 水 | 浓硫酸 |
| D | CaCO3和稀盐酸制取收集 纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 250 mL 1 mol•L-1FeCl3溶液中,阴、阳离子总数为NA | |
| B. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 0.1mol HCN分子中含有的π键数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | 放热1940kJ | B. | 吸热1940kJ | C. | 放热485kJ | D. | 吸热485kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某研究性学习小组设计了一组实验探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:
某研究性学习小组设计了一组实验探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 阳极的电极反应式:4OH--4e-═O2↑+2H2O | |
| B. | 若将阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室,同样可制得纯净物的H3PO2 | |
| C. | H3PO2分子中P元素的化合价为+1价 | |
| D. | 阳极室的H+穿过阳膜扩散至产品室,原料室的H2PO2-穿过阴膜扩散至产品室,二者反应生成H3PO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com