
分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$结合物质的构成计算.
解答 解:(1)由分子构成可知含有相同氧原子数的CO和CO2,其物质的量之比为2;1,设物质的量分别为2mol、1mol,则则质量比为:2mol×28g/mol:1mol×44g/mol=14:11,同温同压下的体积比为2:1,
故答案为:14:11;2:1;
(2)n(RO2)=$\frac{0.448L}{22.4L/mol}$=0.02mol,M(RO2)=$\frac{1.28g}{0.02mol}$=64g/mol,R的相对原子质量为64-2×16=32,
故答案为:64 g/mol;32.
点评 本题考查有关物质的量的计算,明确质量、体积、物质的量、摩尔质量、摩尔体积的关系即可解答,难度不大.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:解答题
 乙酸正丁酯是一种重要化工原料,某实验小组利用图1、图2装置合成乙酸正丁酯(夹持装置已略去),发生的化学反应为:
乙酸正丁酯是一种重要化工原料,某实验小组利用图1、图2装置合成乙酸正丁酯(夹持装置已略去),发生的化学反应为:| 相对分子质量 | 沸点/℃ | 密度(g/cm3) | 水中溶解度 | |
| 正丁醇 | 74 | 117.2 | 0.80 | 微溶 |
| 乙酸 | 60 | 118.1 | 1.05 | 易溶 |
| 乙酸正丁酯 | 116 | 126.5 | 0.90 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③中的氧化产物分别是I2、Fe3+、CoCl2 | |
| B. | 根据以上方程式可以得到氧化性Cl2>Fe3+>Co2O3 | |
| C. | 在③反应中当1molCo2O3参加反应时,2molHCl被氧化 | |
| D. | 可以推理得到Cl2+FeBr2═FeCl2+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.6mol/L | D. | 0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
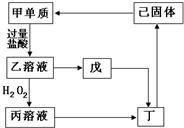 已知甲、乙、丙、丁、戊、己六种物质中含同一种元素,它们之间的转化关系如图所示.其中,丁是一种红褐色沉淀,戊是一种白色沉淀.请回答下列问题:
已知甲、乙、丙、丁、戊、己六种物质中含同一种元素,它们之间的转化关系如图所示.其中,丁是一种红褐色沉淀,戊是一种白色沉淀.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含0.1 mol Na+、0.2 mol Mg2+、0.1 mol Cl-和0.1 mol NO3-的溶液 | |
| B. | 只含0.1 mol NH4+、0.1 mol Ca2+、0.1 mol CO32-和0.1 mol Cl-的溶液 | |
| C. | 为了通过测定pH的大小,达到比较HCl和CH3COOH酸性强弱的目的,分别配制100 mL 0.1 mol/L的NaCl溶液和CH3COONa溶液 | |
| D. | 仅用1 000 mL的容量瓶、烧杯、玻璃棒、量筒、58.5 g NaCl固体和水配制1 L 1 mol/L的NaCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com