
【题目】在一固定容积的密闭容器中,保持一定条件下进行以下反应:A(g)+2B(g)![]() 3C(g)+D(s),已知加入1 molA和3molB。达到平衡后,生成 W mol C。
3C(g)+D(s),已知加入1 molA和3molB。达到平衡后,生成 W mol C。
(1)在相同实验条件下,若在原平衡的基础上,向容器中再加入1 mol A和3 mol B,达到平衡后,C的物质的量为_____________mol。
(2)在相同实验条件下,若在同一容器中改为加入1.5 mol A、6.0 mol B、xmol C和足量的D,若要求在反应混合气体中C体积分数不变,计算x的值为________。
(3)在相同实验条件下,若在同一容器中改为加入0.8 mol A、a mol B、b mol C和足量的D,若要使平衡时C为1.2W mol,则a=________,b=________。
【答案】2W 4.5 2.8 1.2
【解析】
(1)恒温恒容,反应前后气体体积不变,对应物质按相同的比例加入,平衡等效,物质的转化率相同,平衡时对应组分的含量相同;
(2)体积分数仍与原平衡相同,说明为等效平衡,恒温恒容,反应前后气体体积不变,按化学计量数转化到左边,A、B的物质的量之比满足1:3,则与原平衡等效;
(3)在相同实验条件下,若要使平衡时C为1.2W mol,则起始量按化学计量数转化到左边,A、B的物质的量之比满足1:3,且为加入1 molA和3molB的1.2倍关系。
(1)恒温恒容,反应前后气体体积不变,加入2molA和6molB,A、B的物质的量之比为1:3,与原平衡相同,为等效平衡,物质的转化率相同,平衡时对应组分的含量相同,C在反应混合气中的体积分数不变,C的物质的量变为2 W mol。
故答案为:2 W;
(2)恒温恒容,反应前后气体体积不变,按化学计量数转化到左边,A、B的物质的量之比满足1:3,则: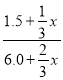 =
=![]() ,解得n=4.5。
,解得n=4.5。
故答案为:4.5;
(3)在相同实验条件下,若要使平衡时C为1.2W mol,则起始量按化学计量数转化到左边,A、B的物质的量之比满足1:3,且为加入1 molA和3molB的1.2倍关系。则:0.8+![]() =1.2,a+
=1.2,a+![]() =3.6,解得:b=1.2,a=2.8,
=3.6,解得:b=1.2,a=2.8,
故答案为:2.8;1.2。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有机化合物G是合成维生素类药物的中间体,其结构简式如图1所示,G的合成路线如图2所示:
其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知:-CHO+
请回答下列问题:
(1)G的分子式是__,G中官能团的名称是__;
(2)第①步反应的化学方程式是__;
(3)B的名称(系统命名)是__;
(4)第②~⑥步反应中属于取代反应的有__(填步骤编号);
(5)第④步反应的化学方程式是________;
(6)写出同时满足下列条件的E的所有同分异构体的结构简式__,①只含一种官能团;②链状结构且无﹣O﹣O﹣;③核磁共振氢谱只有2种峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,在一个体积为2L密闭容器中加入反应物A、B,发生如下反应:A(s)+2B(g)![]() 3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是
3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是
物质 | 起始 | 2分钟 | 4分钟 | 6分钟 |
A | 2 mol | 1.2 mol | ||
B | 6 mol | 3.0 mol | ||
C | 0 mol | x mol | 4.5 mol |
A. 前2分钟内,A的反应速率为0.2molL-1min-1
B. 表中x的值为3.6
C. 4分钟时,反应达到平衡状态,此时正、逆反应的速率都为0
D. 升高温度,正、逆反应的速率都会增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向20 mL N mol·L-1CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如图所示。下列说法中,正确的是

A.a点c(CH3COOH)=10-3mol·L-1
B.b点溶液中离子浓度大小满足关系: c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.c点溶液中离子浓度大小满足关系: c(Na+)+c(OH-)=c(H+)+c(CH3COO-)
D.滴定过程中不可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法回收WC和制备Co2O3的工艺流程简图:

已知:在上述流程中,各种金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Co2+ |
开始沉淀的pH | 1.9 | 7.0 | 6.5 |
沉淀完全的pH | 3.2 | 9.0 | 9.4 |
回答下列问题:
(1)通入氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择的pH的范围是_______。
(2)已知:Ksp(CoCO3)=1.4×10-13,Ksp(CoC2O4)=6.3×10-8。若仅从沉淀转化角度考虑,在0.01mol/L Na2C2O4溶液中加入CoCO3固体能否转化为CoC2O4沉淀?通过计算说明:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发酵法制酒精的过程可粗略表示如下:
①(C6H10O5)n+nH2O![]() nC6H12O6 ②C6H12O6
nC6H12O6 ②C6H12O6![]() 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
(1)上述化学方程式中(C6H10O5)n可能表示_____ ____(填物质名称);
(2)C6H12O6名称是_________,常用_____ ____试剂来检验其存在;
(3)为检验苹果成熟过程中发生了反应①,可在青苹果汁中滴加碘酒,溶液呈_________色,向熟苹果汁中加入Cu(OH)2悬浊液,加热,反应生成____ ____(填实验现象);
(4)下列作用不属于水解反应的是_________
A.吃馒头时多咀嚼后有甜味
B.淀粉溶液和稀硫酸共热一段时间后,滴加碘水不显蓝色
C.不慎将浓硝酸沾到皮肤上会出现黄色斑痕
D.油脂与氢氧化钠溶液共煮后可以制得肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月9日中国科学院正式向社会发布113号、115号、117号和118号元素的中文名称。已知117号元素有多种原子,如![]() 、
、![]() 等。下列说法正确的是
等。下列说法正确的是
A. ![]() 和
和![]() 的化学性质完全不同
的化学性质完全不同
B. 元素Ts的相对原子质量为![]()
C. 基态![]() 原子核外电子共占据7个能级
原子核外电子共占据7个能级
D. Ts位于周期表的第七周期ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的资源化利用能有效减少CO2排放,充分利用碳资源。CaO可在较高温度下捕集CO2,在更高温度下将捕集的CO2释放利用。CaC2O4·H2O热分解可制备CaO,CaC2O4·H2O加热升温过程中固体的质量变化见图。

①写出400~600 ℃范围内分解反应的化学方程式:________。
②与CaCO3热分解制备的CaO相比,CaC2O4·H2O热分解制备的CaO具有更好的CO2捕集性能,其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是( )
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuSO4 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com