
【题目】已知反应NO2(g)+CO(g)=NO(g)+CO2(g)的能量变化如图所示,下列说法正确的是
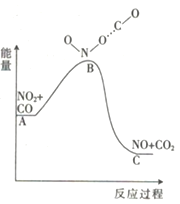
A. 图中A→B的过程为放热过程
B. 该反应为氧化还原反应
C. 1molNO2和1molCO的键能总和大于1molNO和1molCO2的键能总和
D. 1molNO2(g)和1molCO(g)的总能量低于1molNO(g)和1molCO2(g)的总能量
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
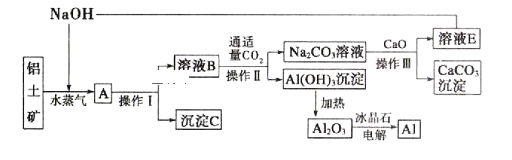
请回答下列问题。
(1)沉淀C的化学式为_______________,该物质除了用于金属冶炼以外,还可用作____________。
(2)电解熔融的氧化铝时,若得到22.4L(标准状况下)![]() ,则同时生成___________g铝。
,则同时生成___________g铝。
(3)操作I、操作II和操作III都是__________(填操作名称),实验室要洗涤,![]() 沉淀应该在____________装置中进行,洗涤方法是_____________________________。
沉淀应该在____________装置中进行,洗涤方法是_____________________________。
(4)生产过程中,除NaOH、![]() 可以循环利用外,还可以循环利用的物质有______________(填化学式),用此法制取铝的副产品是_______________(填化学式)。
可以循环利用外,还可以循环利用的物质有______________(填化学式),用此法制取铝的副产品是_______________(填化学式)。
(5)写出![]() 溶液与CaO反应的离子方程式:_________________________。
溶液与CaO反应的离子方程式:_________________________。
(6)若铝土矿中还含有二氧化硅,此生产过程中得到的氧化铝中将混有杂质_______________(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2常温下是深红棕色液体),设计了如下流程图:
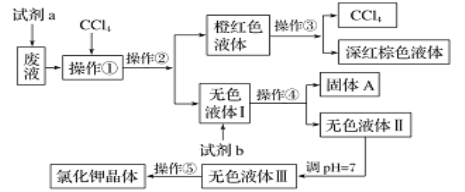
已知:可供选择的试剂 a、试剂b(试剂 b代表一组试剂)如下:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液(H+)、KMnO4溶液(H+)、稀盐酸。请根据流程图,回答相关问题:
(1)若试剂a为H2O2溶液(H+),已知H2O2 + 2KBr + 2HCl = Br2 + 2H2O + 2KCl
①发生反应的离子方程式为:__________;
②每消耗0.2molH2O2,反应转移的电子数为______mol;
③还原剂和还原产物的物质的量之比是_______;
(2)操作①②③④⑤对应的名称分别是:______、分液、_____、过滤、______ ;
(3)为了除去无色液体I中的Ca2+、Mg2+、SO42-,从可供选择的试剂中选出试剂b所代表的物质,按滴加顺序依次是____、____、____(填化学式);
(4)调pH=7是为了除去杂质离子________和_________,以提高氯化钾晶体的纯度;
(5)操作⑤中用到的瓷质仪器名称是_________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于取代反应的是( )
A. 乙烯与水反应生成乙醇 B. 甲烷与氯气反应生成一氯甲烷
C. 乙醇与氧气反应生成乙醛 D. 乙烯与高锰酸钾溶液反应生成CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在科学史上中国有许多重大的发明和发现,它们为世界的现代化奠定了基础,以下发明和发现属于化学史上中国对世界的贡献的是( )
①火药 ②指南针 ③造纸 ④印刷技术 ⑤炼铜、炼铁、炼钢 ⑥合成有机高分子材料 ⑦人工合成蛋白质 ⑧提出原子-分子学说
A.②③⑥⑧B.①③⑤⑦C.④⑤⑦⑧D.①③④⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素 X、Y、Z 和 W 在元素周期表中的位置如图所示,原子序数之和为 48。下列有关说法中正确的是
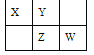
A. 原子半径(r)大小比较 r(X)< r(Y)
B. Z 和 Y 可形成共价化合物 YZ3
C. W 的非金属性比 Z 的强,所以 W 的简单气态氢化物的沸点比 Z 的高
D. W 的最低价单核阴离子的失电子能力比 X 的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A. 气体甲一定是纯净物 B. 沉淀甲是硅酸和硅酸镁的混合物
C. K+、AlO和SiO一定存在于溶液X中 D. CO和SO一定不存在于溶液X中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com