
【题目】1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均釆用虚线表示。
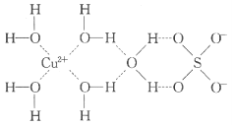
(1)写出基态Cu原子的核外电子排布式____,S原子的价层电子排布图______
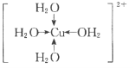
(2)写出胆矾晶体中水合铜离子的结构简式_____(必须将配位键表示出来)。
(3)向CuSO4溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式_____。比较NH3和[Cu(NH3)4]2+中H-N-H 中键角的大小:NH3_____[Cu(NH3)4]2+(填“![]() ” “
” “![]() ” 或“=”)。
” 或“=”)。
(4)已知H2O2的结构如图:
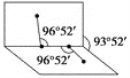
H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,估计它难溶于CS2,简要说明原因______。
(5)分析下表中两种物质的键能数据(单位:kJ/mol)。
A—B | A=B |
| |
CO | 357.7 | 798.9 | 1 071.9 |
N2 | 154.8 | 418.4 | 941.7 |
结合数据说明CO比N2活泼的原因:_________。
【答案】1s22s22p63s23p63d104s1或[Ar]3d104s1 ![]()
 [Cu(NH3)4]SO4H2O < 因H2O2为极性分子,而CS2为非极性溶剂,根据相似相溶规律,H2O2难溶于CS2中 CO中第一个断裂的π键的键能是273kJ/mol,N2中第一个断裂的π键的键能是523.3kJ/mol,所以CO的第一个键比N2更容易断
[Cu(NH3)4]SO4H2O < 因H2O2为极性分子,而CS2为非极性溶剂,根据相似相溶规律,H2O2难溶于CS2中 CO中第一个断裂的π键的键能是273kJ/mol,N2中第一个断裂的π键的键能是523.3kJ/mol,所以CO的第一个键比N2更容易断
【解析】
(1)铜是29号元素,其原子核外有29个电子,根据构造原理书写其基态原子核外电子排布式;硫是16号元素,其核外电子排布式为1s22s22p63s23p4,根据价电子排布式3s23p4书写其价层电子排布图;
(2) CuSO45H2O中铜离子含有空轨道,水分子含有孤对电子对,铜离子与水分子之间形成配位键,铜离子配体数为4;
(3)硫酸铜加氨水生成的深蓝色物质是铜氨络合离子,析出的晶体是铜氨络合物。由于NH3提供孤对电子与Cu2+形成配位键后,N-H成键电子对受到的排斥力减小,所以H-N-H键角增大;
(4)判断H2O2、CS2分子的极性,依据相似相溶的原理解答;
(5)根据断裂三键中的中的一个![]() 键消耗的能量判断。
键消耗的能量判断。
(1)铜是29号元素,其原子核外有29个电子,根据构造原理知,其基态原子核外电子排布式为:1s22s22p63s23p63d104s1或[Ar]3d104s1,硫原子核外电子排布式为1s22s22p63s23p4,价电子排布式3s23p4,则其价层电子排布图为![]() ;
;
因此,本题正确答案是:1s22s22p63s23p63d104s1或[Ar]3d104s1;![]() ;
;
(2) CuSO45H2O中铜离子含有空轨道,水分子含有孤对电子对,铜离子与水分子之间形成配位键,铜离子配体数为4。水合铜离子的结构简式为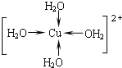 ,
,
因此,本题正确答案是: ;
;
(3)向深蓝色透明溶液加入乙醇,由于乙醇能降低溶解度,有利于晶体析出,所以[Cu(NH3)4]SO4H2O在乙醇中的溶解度小于在水中的溶解度,故会析出深蓝色的晶体:[Cu(NH3)4]SO4H2O;由于NH3提供孤对电子与Cu2+形成配位键后,N-H成键电子对受到的排斥力减小,所以H-N-H键角增大,所以键角的大小:NH3<[Cu(NH3)4]2+,
因此,本题正确答案是:[Cu(NH3)4]SO4H2O;<;
(4)相似相溶原理是指由于极性分子间的电性作用,使得极性分子组成的溶质易溶于极性分子组成的溶剂,难溶于非极性分子组成的溶剂;非极性分子组成的溶质易溶于非极性分子组成的溶剂,难溶于极性分子组成的溶剂,H2O2是极性分子,CS2是非极性分子,依据相似相溶的原理可知,H2O2难溶于CS2,
因此,本题正确答案是:因H2O2为极性分子,而CS2为非极性溶剂,根据相似相溶规律,H2O2难溶于CS2中;
(5)根据表中数据可知,断裂C≡O中的一个π键消耗的能量是1071.9kJ/mol-798.9kJ/mol=273kJ/mol,断裂N≡N中的一个π键消耗的能量是941.7kJ/mol-418.4kJ/mol=523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼,
因此,本题正确答案是:CO中第一个断裂的π键的键能是273kJ/mol,N2中第一个断裂的π键的键能是523.3kJ/mol,所以CO的第一个键比N2更容易断。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下图为周期表中的一部分,若a原子最外层电子数比次外层电子数少3个,则下列说法不正确的是
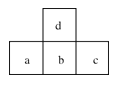
A.a、b、c最高价氧化物对应的水化物的酸性强弱关系是c>b>a
B.a、b、c的氢化物水溶液的酸性强弱关系是a<b<c
C.a和d的原子结合可以形成带3个单位负电荷的阴离子
D.原子半径由大到小的顺序是c>b>d>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N—N—N键角都是108.1°,下列有关N(NO2)3的说法不正确的是( )
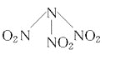
A. N(NO2)3分子中既含极性键又含非极性键
B. 分子中四个氮原子共平面
C. 该物质既有氧化性又有还原性
D. 15.2 g该物质含有6.02×1023个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。

请回答下列问题:
(1)实验室制取氨气的化学方程式为_________;
(2)装置A中的烧瓶内固体不可以选用________(选填序)
A.生石灰 B.碱石灰 C.五氧化二磷 D.烧碱
(3)装置F中发生反应的离子方程式是_________;
(4)B装置的作用_________;E装置的作用_________;
(5)若装置C内出现浓厚的白烟并在容器内壁凝结,且另一生成物是空气的主要成分之一。请写出反应的化学方程式:_________;
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,可以将尾气通入盛有_________溶液的烧杯来处理。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式不正确的是
A.小苏打溶液中加入醋酸的离子方程式:CH3COOH+HCO3-=CH3COO-+H2O+CO2↑
B.植物光合作用的化学方程式:6H2O+6CO2![]() C6H12O6+6O2
C6H12O6+6O2
C.碳酸钠水解的离子方程式:CO32-+2H2O=H2CO3+2OH-
D.一水合氨在水中的电离方程式:NH3·H2ONH4++OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了证明一水合氨(NH3H2O)是弱电解质,常温下做以下实验没有意义的是
A.用pH试纸测得0.010 mol/L氨水的pH为10
B.用pH试纸测得0.10mol/L NH4Cl溶液的pH<7
C.比较浓度均为 0.1 mol·L-1NaOH溶液和氨水的导电能力
D.取10mL 0.010mol/L氨水,滴入2滴酚酞,显粉红色,再滴加少量稀盐酸,颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图示装置的叙述不正确的是( )
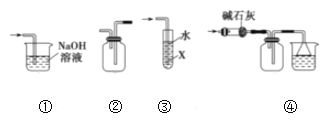
A.①可用于吸收实验中多余的SO2
B.②可用于收集H2、NH3、Cl2、NO等
C.③中X为CC14,可用于吸收NH3或HC1气体
D.④可用于收集NH3,并吸收多余的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法正确的是( )
A.1mol乙醇所含共价键数目为6NA
B.22.4LC2H4和C2H6混合气体含有的碳原子数是2NA
C.18g葡萄糖分子中含羟基数目为0.6NA
D.标准状况下,6g乙酸和丙醇(C3H8O)的混合物中含有的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2 等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
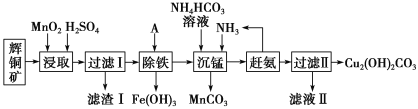
已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
②Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有____(任写一种)。
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:____。
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为____,若加 A 后溶液的 pH调为5,则溶液中 Fe3+的浓度为____mol/L。
(4)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:____。
(5)“赶氨”时,最适宜的操作方法是____。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是____(写化学式)。
(7)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com