
分析 强电解质在溶液中完全电离,电离方程式用等号,弱电解质在溶液中部分电离,电离方程式用可逆号,先判断强弱电解质,然后根据电离方程式的书写原则进行解答.
解答 解:①氢氧化钡为强电解质,在溶液中完全电离,其电离方程式为:Ba(OH)2=Ba2++2OH-,
故答案为:Ba(OH)2=Ba2++2OH-;
②硫酸铝为强电解质,在溶液中完全电离出铝离子和硫酸根离子,其电离方程式为:Al2(SO4)3=2Al3++3SO42-,
故答案为:Al2(SO4)3=2Al3++3SO42-;
③硝酸为强电解质,在溶液中完全电离,其电离方程式为:HNO3=H++NO3-,
故答案为:HNO3=H++NO3-;
④碳酸钠为强电解质,在溶液中完全电离出钠离子和碳酸根离子,其电离方程式为:Na2CO3=2Na++CO32-,
故答案为:Na2CO3=2Na++CO32-;
⑤NaHSO4在溶液中完全电离出钠离子、氢离子和硫酸根离子,其电离方程式为:NaHSO4=Na++H++SO42-,
故答案为:NaHSO4=Na++H++SO42-;
⑥H2SO4为二元强酸,其电离方程式为:H2SO4=2H++SO42-,
故答案为:H2SO4=2H++SO42-;
⑦醋酸钠在溶液中完全电离出钠离子和醋酸根离子,其电离方程式为:CH3COONa=CH3COO-+Na+,
故答案为:CH3COONa=CH3COO-+Na+;
⑧BaSO4为强电解质,溶于水的硫酸钡完全电离,其电离方程式为:BaSO4=Ba2++SO42-,
故答案为:BaSO4=Ba2++SO42-.
点评 本题考查了电离方程式的书写方法,题目难度不大,正确判断强弱电解质为解答关键,注意掌握电离方程式的书写原则想,试题培养了学生的规范答题能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016-2017学年甘肃省高二上第一次学段考试化学卷(解析版) 题型:选择题
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应中和热ΔH=-57.3 kJ·mol-1,H2SO4和Ba(OH)2反应热ΔH=2×(-57.3)kJ·mol-1
B.1 mol甲烷燃烧生成气态水和二氧化碳气体所放出的热量就是甲烷的燃烧热
C.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0 kJ·mol-1
D.需要加热才能发生的反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
用pH试纸测定某无色溶液的pH时,规范的操作是(  )
)
A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B.将溶液倒在pH试纸上,跟标准比色卡比较
C.用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较
D.在试管内放入少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5Cl2+I2+6H2O═10HCl+2HIO3 | |
| B. | 2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)+2H2O | |
| C. | MnO2+4HCI$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ | |
| D. | 2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$2NaOH++Cl2↑+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 利用如图装置,写出除去下列物质中的杂质的方法,并写出化学方程式(括号内的气体为杂质).
利用如图装置,写出除去下列物质中的杂质的方法,并写出化学方程式(括号内的气体为杂质).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
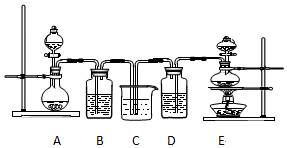

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
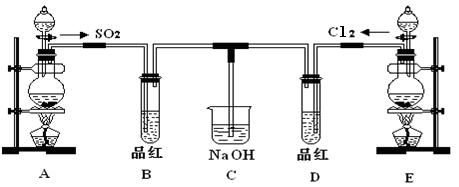
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO2 | CO | |||
| A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| C | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com