
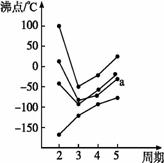
图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是
A.HI
B.SbH3
C.H2Te
D.SiH4
科目:高中化学 来源: 题型:
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德。某种兴奋剂的结构简式如图所示。有关该物质的说法正确的是
A.该物质与苯酚属于同系物, FeCl3溶液呈紫色
B.滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C.1 mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4 mol和7 mol.
D.分子中的所有碳原子不可能共平面

查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两种金属元素:①与稀盐酸反应,甲比乙反应剧烈;②甲原子能与乙的阳离子发生置换反应;③甲的最高价氧化物对应的水化物碱性比乙的最高价氧化物对应的水化物碱性强;④甲与乙用导线连接浸入稀硫酸形成原电池,电流由乙到甲;⑤甲单质的熔沸点比乙的低。能说明甲的金属性比乙强的是 ( )
A.只有②③ B.只有②③⑤ C.只有①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
通过复习总结,你认为下列对化学知识概括合理的是
A.能跟酸反应的氧化物,都是碱性氧化物
B.凡具有正四面体结构的分子中,其键角均为109°28′
C.有新单质生成的化学反应一定都是氧化-还原反应
D.核外电子总数相同的原子,一定是同种元素的原子
查看答案和解析>>
科目:高中化学 来源: 题型:
具有下列电子层结构的原子或离子,其对应的元素在周期表中的位置说法正确的是
A.最外层电子排布为1s2的原子和最外层电子排布为2s2的原子,所对应的两元素一定在同一主族
B.3p能级上有1个空轨道的原子和4p能级上有1空轨道的原子,所对应的两元素一定在同一主族
C.最外层电子排布为nsnnpn的原子和最外层电子排布为2s22p6的离子,所对应的两元素一定在同一周期
D.原子核外M层上的s能级和p能级都填满了电子,而d轨道上尚未有电子的两种原子,所对应的两元素一定在同一周期
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的A、B、C、D、E、F、G七种前四周期元素(稀有气体除外),常温下,有三种元素对应的单质呈气态,C与D同族。其中A原子核外有六种不同运动状态的电子,C为地壳中含量做多的元素,F的简单离子是同周期主族元素形成的简单离子中氧化性最弱的,G的基态原子的最外能层只有一个电子,其他能层均已充满电子。
(1)电负性越大的原子,对键合电子的吸引能力越强,通常对应元素化合价呈现负价。根据B、C、D、E四种元素形成的常见化合物的化合价,确定电负性最大的元素,写出其基态原子的电子排布图 。
(2)甲是由B元素等非金属元素组成的离子化合物,甲可由E的氢化物溶液与电解质乙溶液反应生成,写出该反应的离子方程式 。
(3)A元素可形成多种单质,一种晶体结构如图一所示,该晶体与熔融的F单质相互作用,形成某种青铜色的物质(其中的元素F用“●”表示),原子分布如图二所示,该物质的化学式为 。另一种的晶胞如图三所示,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为___________g·cm-3(保留两位有效数字)。
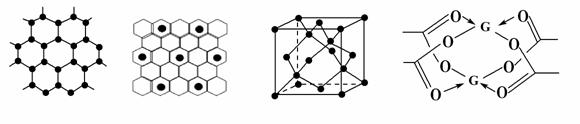 图一 图二 图三 图四
图一 图二 图三 图四
(4)G元素形成的单质,其晶体的堆积模型为________,G的醋酸盐晶体局部结构如图四,该晶体中含有的化学键是________(填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(5)E和F与不同价态的G可组成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均是由G和E两元素形成的无限长链结构(如下图),已知其中一种化合物的化学式为FGE3,另一种的化学式为 。

(6)若物质F2D3是一种含有非极性共价键的离子化合物,各原子最外层都满足8e-稳定结构,请你写出该化合物阴离子的电子式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.原子最外层电子数等于或大于3(小于8)的元素一定是非金属元素
B.原子最外层只有1个电子的元素一定是金属元素
C.最外层电子数比次外层电子数多的元素一定位于第二周期
D.某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,质量分数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g,该温度下NaOH的溶解度为S。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为______________________________。
(2)用c、d来表示该温度下NaOH的溶解度(S)为_____________________________。
(3)用m、V表示溶液中溶质的物质的量浓度(c)为____________________________。
(4)用w、d表示溶液中溶质的物质的量浓度(c)为_____________________________。
(5)用c、d表示溶液中溶质的质量分数(w)为_________________________________。
(6)用S表示溶液中溶质的质量分数(w)为____________________________________。
(7)用S、d表示溶液中溶质的物质的量浓度(c)为______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com