
| A. | 在标准情况下,22.4LH2O含有的分子数为NA | |
| B. | 1L 0.1 mol?L-1的MgCl2溶液中含Mg2+的数目为0.1NA | |
| C. | 17.6g丙烷中所含的共价键数目为4NA | |
| D. | 20 ml 2mol?L-1 H2O2完全分解,转移的电子数为0.08NA |
分析 A.气体摩尔体积使用对象为气体;
B.镁离子水溶液中部分水解;
C.依据n=$\frac{m}{M}$计算丙烷的物质的量,结合1个丙烷分子含有8个C-H,2个C-C;
D.双氧水分解时,1mol双氧水转移1mol电子.
解答 解:A.标况下水是液体,不能使用气体摩尔体积,故A错误;
B.镁离子水溶液中部分水解,所以1L 0.1 mol?L-1的MgCl2溶液中含Mg2+的数目小于0.1NA,故B错误;
C.17.6g丙烷物质的量为0.4mol,每摩尔丙烷中含有共价键10mol,所以0.4mol丙烷含共价键为4mol,即4NA,故C正确;
D.双氧水分解时,1mol双氧水转移1mol电子,故20mL2mol/L的双氧水即0.04mol双氧水分解转移0.04NA个电子,故D错误;
故选:C.
点评 本题考查阿伏加德罗常数的应用,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | B、C、D离子的半径大小是D>B>C | |
| B. | C的单质能将F单质从AF的溶液中置换出来 | |
| C. | 氧化物对应的水化物的酸性:B<F | |
| D. | B与C能存在F同一离子化合物中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 g铁与盐酸反应时失去的电子数目为0.3 NA | |
| B. | 71 g氯气所含原子数目为NA | |
| C. | 标准状况下,以任意比混合的氮气和氧气11.2 L,所含的分子数为0.5 NA | |
| D. | 在25℃,1.01×105Pa时,22.4 L氢气所含的原子数目为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
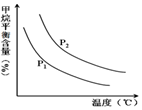 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
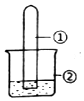 用图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用图所示装置进行下列实验,实验结果与预测的现象不一致的是( )| 选项 | ①中的物质 | ②中的物质 | 预测装置中现象 |
| A | NO2 | 蒸馏水 | 试管充满无色溶液 |
| B | SO2 | 紫色石蕊溶液 | 溶液逐渐变为红色 |
| C | NH3 | AlCl3溶液 | 产生白色沉淀 |
| D | Cl2 | AgNO3溶液 | 产生白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO 3-═3Fe 3++2H2O+NO↑ | |
| B. | 氧化亚铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| C. | 固体氯化钠与浓硫酸混合加热:H 2SO 4+2Cl-═SO 2↑+Cl 2↑+H 2O | |
| D. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 天津港爆炸事故救援过程中,消防员若发现存放金属钠、电石、甲苯二异氰酸酯等化学品的仓库起火,应立即用泡沫灭火器将火扑灭 | |
| B. | 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,说“纳米铜”的还原性比铜片更强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 80 mL10 mol/L的浓盐酸与足量MnO2反应,转移电子数为0.4 NA | |
| B. | 通入了1 mol Cl2的新制氯水中,HC1O、Cl-、C1O-粒子数之和为2NA | |
| C. | 1 mol Na2O2中含有的阴离子数为2 NA | |
| D. | 标准状况下,4.48L NH3中共用电子对数为0.6 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铁锅生锈过程中有原电池反应,负极反应式是:Fe-2e-=Fe2+ | |
| B. | 铁锅生锈过程中有Fe(OH)3生成:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 摄入体内的铁锈会在胃内产生不利于健康的Fe3+:Fe2O3+6H+═2Fe3++3H2O | |
| D. | 用醋可除去铁锈:6CH3COOH+Fe2O3═6CH3COO-+2Fe3++3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com