
【题目】如图为实验室制取和收集纯净干燥的氯气,并进行氯气性质探究的实验装置图:
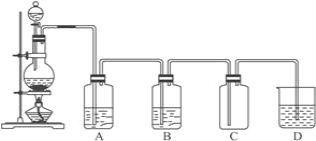
(1)反应前,在__________中装浓盐酸(填写仪器名称),__________中装MnO2(填写仪器名称)
(2)装置A中所装试剂是______,装置B中所装的试剂是_____________。
(3)装置D中所装试剂是______,发生反应的化学方程式为______________________。
(4)实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度______________。
【答案】 分液漏斗 圆底烧瓶 饱和食盐水 浓硫酸 NaOH溶液 Cl2+2NaOH==NaCl+NaClO+H2O 11.9mol/L
【解析】本题考查实验方案设计与评价,(1)此反应是固体与液体反应制备气体,浓盐酸应盛放在分液漏斗中,圆底烧瓶盛装MnO2;(2)实验目的是制取和收集纯净的氯气,以及验证氯气的性质,MnO2与浓盐酸反应制取的氯气中混有HCl和水蒸气,装置A的作用是除去HCl,即装置A中盛放的是饱和食盐水,装置B的作用是除去氯气中水蒸气,装置B盛放的是浓硫酸;(3)装置C是收集氯气,氯气有毒,必须尾气处理,装置D的作用是除去过量的氯气,即装置D中盛放NaOH溶液;发生的化学反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O;(4)根据c=1000ρω%/M=1000×1.19×36.5%/36.5mol·L-1=11.9mol·L-1。


科目:高中化学 来源: 题型:
【题目】两种元素的核外电子层数之比与最外层电子数之比相等,则在核电荷数1~10的元素中,满足上述关系的元素共有( )
A.1对B.2对C.3对D.4对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlCl3是一种催化剂,某校学习小组用下面装置制备少量AlCl3。已知:AlCl3遇到空气中的水蒸气时能剧烈反应生成Al(OH)3和HCl;AlCl3在180℃时升华。根据要求完成下列问题:
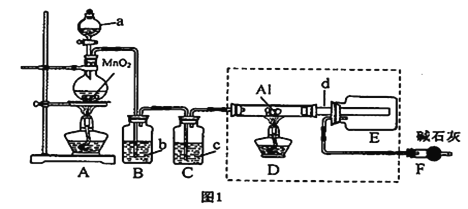
(1)A装置中反应的化学方程式为____________________________。
(2)试剂b为______________。
(3)所用d导管较粗的原因是______________;E装置的作用为______________。
(4)F装置的作用为______________。
(5)若图l中的D、E装置改为下面装置,D装置中的现象为_____________________;用离子方程式表示E中的现象变化____________________________。
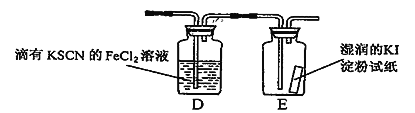
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向容积为2L的密闭器中充入2molA气体和1molB气体,在一定条件下发生如下反应:2A(g)+B(g)3C(g);经2s后达到平衡,测得C气体的浓度为0.6molL﹣1 . 下列说法中正确的是( )
①用物质A表示该反应的平均反应速率为0.2molL﹣1s﹣1
②用物质B表示该反应的平均反应速率为0.2molL﹣1s﹣1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2molL﹣1
⑤其它条件不变,向容器中再加入1molC气体,达到新平衡时,C的体积分数不变.
A.①②③
B.①③⑤
C.②④⑤
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氮的固定的是
①N2和H2在一定条件下反应生成NH3
②雷雨闪电时空气中的N2和O2化合生成NO
③NH3经过催化氧化生成NO
④NH3和HNO3反应生成NH4NO3
A.①③B.②④C.③④D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学利用下图装置对电解氯化铜实验进行了研究。
装置 | 现象 |
| 电解一段时间时,阳极石墨表面产生气体,阴极石墨上附着红色物质,烧杯壁变热,溶液由蓝色变为绿色 |
(1)甲认为电解过程中阳极产生的是溶液变绿的原因,写出产生该物质的电极反应式:。
(2)乙查阅资料,CuCl2溶液中存在平衡:Cu2+ + 4Cl ![]() [CuCl4]2_(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2_(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2_浓度增大的原因:。
[CuCl4]2_(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2_(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2_浓度增大的原因:。
(3)丙改用下图装置,在相同条件下电解CuCl2溶液,对溶液变色现象继续探究。
装置 | 现象 |
| 电解相同时间时,阳极石墨表面产生气泡,溶液仍为蓝色;阴极石墨上附着红色物质,溶液由蓝色变为绿色;U型管变热,冷却后阴极附近溶液仍为绿色 |
丙通过对现象分析证实了甲和乙的观点均不是溶液变绿的主要原因。丙否定甲的依据是 , 否定乙的依据是。
(4)丙继续查阅资料:
i. 电解CuCl2溶液时可能产生[CuCl2]_ , [CuCl2]_掺杂Cu2+后呈黄色
ii. 稀释含[CuCl2]_的溶液生成CuCl白色沉淀据此丙认为:电解过程中,产生[CuCl2]_掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。
丙进行如下实验:
a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]_的黄色溶液。
c. 冷却后向上述溶液……
d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
① a的目的是。
② 写出b中生成[CuCl2]_的离子方程式:。
③ 补充c中必要的操作及现象:。
丙据此得出结论:电解时阴极附近生成[CuCl2]_是导致溶液变绿的原因。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫的下列化学性质中,体现二氧化硫作为还原剂的是
A.SO2在一定条件下与O2反应转化为SO3
B.通入品红溶液中,使品红褪色
C.溶于水形成不稳定的亚硫酸
D.与碱液反应生成亚硫酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,所用仪器合理的是( )
A.用25mL的碱式滴定管量取14.80mLNaOH溶液
B.用100mL量筒量取5.2mL的盐酸
C.用托盘天平称取25.20gNaCl
D.用100mL容量瓶配制50mL1.0mol/L盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com