
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
分析 ①光照条件下通入Cl2,氯气会和乙烷之间发生取代反应;
②饱和碳酸钠溶液可以和乙酸之间发生中和反应;
③苯酚和氢氧化钠反应生成苯酚钠;
④乙醇和水的沸点不同,水可与生石灰反应.
解答 解:①光照条件下通入Cl2,氯气会和乙烷之间发生取代反应,和乙烯之间发生加成反应,这样即将杂质除去,又将要留的物质反应了,不符合除杂的原则,故①错误;
②饱和碳酸钠溶液可以和乙酸之间发生中和反应,但是和乙酸乙酯是互不相溶的,分液即可实现分离,故②正确;
③除去苯中的少量苯酚,向混合物中加入NaOH溶液反应生成苯酚钠,然后分液即可,故③正确;
④乙醇和水的沸点不同,水可与生石灰反应,用蒸馏的方法分离,故④正确.
故选D.
点评 本题考查物质的除杂、混合物的分离提纯,明确物质的性质及常见混合物的分离方法是解答本题的关键,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:解答题
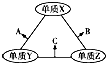 (Ⅰ) W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻、Y与Z相邻; X,Y位于同一主族,它们能组成YX2,YX3两种常见化合物;W元素的氢化物与Z元素的氢化物反应生成盐.请回答下列问题:
(Ⅰ) W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻、Y与Z相邻; X,Y位于同一主族,它们能组成YX2,YX3两种常见化合物;W元素的氢化物与Z元素的氢化物反应生成盐.请回答下列问题: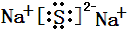 .(用元素符号表示)
.(用元素符号表示)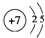 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | |
| 试管1 | 17.5 | 34.9 | 50.1 | 60.3 | 70.4 | 80.2 | 84.9 | 85.2 | 85.4 |
| 试管2 | 21.7 | 41.2 | 57.5 | 70.8 | 81.3 | 84.9 | 85.3 | 85.4 | 85.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸的酸性强于次氯酸,判断硫与氯的非金属性强弱 | |
| B. | 镁与铝分别与物质的量浓度相同的盐酸反应,判断镁与铝的金属活动性强弱 | |
| C. | 钠和镁分别与冷水反应,判断金属活动性强弱 | |
| D. | Cl2与Br2分别与足量的H2反应,判断氯与溴的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沼气和天然气的主要成分都是甲烷 | |
| B. | 石油经过分馏及裂化等工序得到的物质均为纯净物 | |
| C. | 石油的裂解是化学变化,而石油的分馏和煤的干馏是物理变化 | |
| D. | 煤中含有苯和甲苯,可用先干馏后分馏的方法得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:F->Na+>Mg2+>Al3+ | B. | 热稳定性:HF>H2O>H2S | ||
| C. | 还原性:F-<Cl-<I- | D. | 碱性强弱:NaOH>KOH>CsOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com