
【题目】常温下,下列各组离子在相应的条件下能大量共存的是( )
A.由水电离产生的c(H+)=1×10-10molL-1的溶液中:NO3-、Fe2+、Na+、SO42-
B.![]() =10-10molL-1的溶液中:NH4+、I-、Cl-、K+
=10-10molL-1的溶液中:NH4+、I-、Cl-、K+
C.![]() =1×106的溶液中:K+、Na+、Cl-、HCO3-
=1×106的溶液中:K+、Na+、Cl-、HCO3-
D.惰性电极电解AgNO3后的溶液中:SO32-、K+、Na+、S2-
【答案】B
【解析】
A.由水电离产生的c(H+)=1×10-10molL-1的溶液可能是碱性溶液,也可能是酸性溶液。在酸性溶液中,H+、NO3-和Fe2+发生氧化还原不能大量共存,在碱性溶液中,Fe2+和OH-反应生成Fe(OH)2,不能大量共存,A不符合题意;
B.![]() =10-10molL-1<10-7 molL-1,其溶液为酸性溶液,NH4+、I-、Cl-、K+不生成气体,不产生沉淀,也不生成水,可以大量共存,B符合题意;
=10-10molL-1<10-7 molL-1,其溶液为酸性溶液,NH4+、I-、Cl-、K+不生成气体,不产生沉淀,也不生成水,可以大量共存,B符合题意;
C.![]() =1×106的溶液为碱性溶液,HCO3-与OH-反应生成CO32-和H2O,不能大量共存,C不符合题意;
=1×106的溶液为碱性溶液,HCO3-与OH-反应生成CO32-和H2O,不能大量共存,C不符合题意;
D.用惰性电极电解AgNO3溶液,阴极Ag+放电,阳极溶液中的OH-放电,总反应方程式为4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3,溶液中含有HNO3,则SO32-和S2-会与HNO3发生氧化还原,不能大量共存,D不符合题意。
4Ag+O2↑+4HNO3,溶液中含有HNO3,则SO32-和S2-会与HNO3发生氧化还原,不能大量共存,D不符合题意。
答案选B。


科目:高中化学 来源: 题型:
【题目】已知![]() 互为同分异构体,下列说法不正确的是
互为同分异构体,下列说法不正确的是
A. z的二氯代物有三种
B. x、y的一氯代物均只有三种
C. x、y 可使溴的四氯化碳溶液因发生加成反应而褪色
D. x、y、z中只有x的所有原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是某香料的有效成分,其分子中含3个六元环。M的一种合成路线如图:

已知①A(C8H8)分子中所有原子可能共平面;②D的核磁共振氢谱上有6个峰;③H和I互为同系物。请回答下列问题:
(1)A的名称是___,E中所含官能团名称是___。
(2)B→C的反应类型是___。
(3)写出H和I反应生成M的化学方程式:___。
(4)T是H的同分异构体,同时具备下列条件的T有___种(不考虑立体异构),其中,苯环上一溴代物只有2种的结构简式为___。
①遇FeCl3溶液发生显色反应;②能发生水解反应和银镜反应。
(5)乳酸(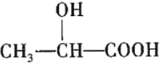 )在医药方面广泛用作防腐剂、载体剂、助溶剂等。参照上述流程,以2-丁烯和乙烯为原料合成乳酸,设计合成路线___(无机试剂任选)。
)在医药方面广泛用作防腐剂、载体剂、助溶剂等。参照上述流程,以2-丁烯和乙烯为原料合成乳酸,设计合成路线___(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿巴卡韦(Abacavir)是一种核苷类逆转录酶抑制剂,存在抗病毒功效。关于其合成中间体 M(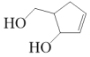 ),下列说法正确的是( )
),下列说法正确的是( )
A.与环戊醇互为同系物B.分子中含有三种官能团
C.能使酸性高锰酸钾溶液和溴水褪色,且原理相同D.可用碳酸钠溶液鉴别乙酸和 M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验在学科中有着非常重要的作用,结合图示实验装置,下列相关分析的描述不正确的是( )
A.图1:盐桥中使用KCl溶液,电子的流向是Zn→G→Cu→CuSO4溶液→盐桥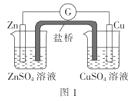
B.图2:可根据该实验验证铁的吸氧腐蚀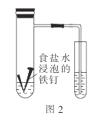
C.图3:在强酸和强碱的中和热实验中,强碱的浓度比强酸的略大
D.图4:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断反应2NO2(g)![]() N2O4(g)是一个放热反应
N2O4(g)是一个放热反应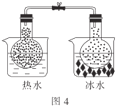
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴、铜及其化合物用途非常广泛。回答下列问题:
(1)基态Br原子核外电子排布式为[Ar]___。
(2)已知反应:Cu(BF4)2.6H2O+Cu+8CH3CN=2[Cu(CH3CN)4]BF4+6H2O。
①配合物[Cu(CH3CN)4]BF4中,与铜形成配位键的原子是___,BF4-的空间构型是___,与BF4-互为等电子体的分子有___(任写一种)。
②CH3CN分子中碳原子的杂化方式是___;1个CH3CN分子中含有___个σ键。
(3)电子亲合能与电离能相对应,元素的气态基态原子获得一个电子成为气态一价负离子所释放的能量称为该元素的第一电子亲合能,其大小主要取决于原子的有效核电荷、原子半径和原子的电子构型等因素。Br与F、Cl位于同一主族,第一电子亲合能(如图1所示)原比氯和溴都小,其原因是___。
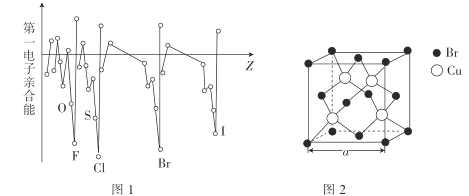
(4)溴化亚铜(晶胞结构如图2所示)可用作有机合成的催化剂,密度为4.71g·cm-3。
①晶胞中Br-的配位数为___。
②晶胞参数a=___(列出表达式即可)nm。(设NA为阿伏加德罗常数的数值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原SiHCl3(沸点:31.85℃)制备纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是( )

A. 装置Ⅱ、Ⅲ中依次盛装的是浓H2SO4、冰水
B. 实验时,应先加热管式炉,再打开盛装稀硫酸的分液漏斗
C. 为鉴定制得的硅中是否含微量铁单质,需要用到的试剂为盐酸、双氧水、硫氰化钾溶液
D. 该实验中制备氢气的装置也可用于氧氧化钠稀溶液与氯化铵固体反应制备氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中的字母分别代表一种化学元素。

(1)上述元素中,原子中未成对电子数最多的是 ___________ (填字母),写出该元素基态原子的核外电子排布式: ___________ 。
(2)根据下表所提供的电离能数据,回答下列问题。
锂 | X | Y | |
I1 | 520 | 496 | 580 |
I2 | 7296 | 4562 | 1820 |
I3 | 11799 | 6912 | 2750 |
I4 | 9543 | 11600 |
①表中X可能为以上13种元素中的 _____________ (填字母)元素。用元素符号表示X和j形成的一种化合物的化学式: _____________ 。
②Y是周期表中第 _____________ 族元素。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu3N具有良好的电学和光学性能在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工程等领域中,发挥着广泛的、不可替代的巨大作用。
(1)C、N、O三种元素的第一电离能由大到小的顺序为__。
(2)与N3-含有相同电子数的三原子微粒的空间构型是__。
(3)Cu+的电子排布式为__,其在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu,但CuO在高温下会分解成Cu2O,试从结构角度解释高温下CuO为何会生成Cu2O:__。
(4)在Cu的催化作用下,乙醇可被空气氧化为乙醛,乙醛分子中碳原子的杂化方式是__,乙醛分子H-C-O的键角_(填“大于”“等于”或“小于”)乙醇分子中的H-C-O的键角。
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代有两种不同的结构,试画出Cu(H2O)2Cl2具有极性的分子的结构式:___。
(6)Cu3N的晶胞结构如图所示,N3-的配位数为__,Cu+的半径为apm,N3-的半径为bpm,Cu3N的密度为__g·cm-3(阿伏加德罗常数用NA表示)。
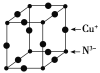
(7)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。肼—空气燃料电池是一种碱性燃料电池,产物无污染,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时,负极的电极反应式是__;
(8)发射神舟飞船的长征火箭用肼(N2H4,气态)为燃料,为了提高肼(N2H4)燃烧过程中释放的能量,常用NO2作氧化剂代替O2,这两者反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ·mol-1;②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1,写出肼和NO2完全反应的热化学方程式:__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com