
 .
. .
. +
+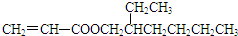 $→_{Na_{2}CO_{3}/NMP}^{Pd/C}$
$→_{Na_{2}CO_{3}/NMP}^{Pd/C}$ 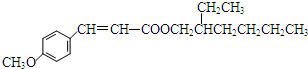 +HBr.
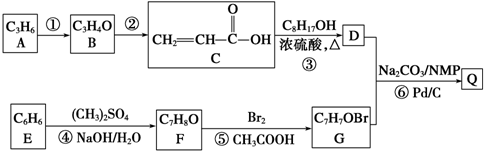
+HBr. 分析 B的分子式为C3H4O,能转化得到CH2=CH-COOH,则B为CH2=CH-CHO,A为CH3CH=CH2.C8H17OH分子中只有一个支链,且为乙基,其连续氧化的产物能与NaHCO3反应生成CO2,分子中存在-CH2OH结构,其消去产物的分子中只有一个碳原子上没有氢,故C8H17OH的结构简式为 ,C与C8H17OH发生酯化反应生成D为
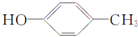
,C与C8H17OH发生酯化反应生成D为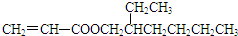 ,由E的分子式可知E为苯,F不能与NaOH溶液反应,不含酚羟基,故F为
,由E的分子式可知E为苯,F不能与NaOH溶液反应,不含酚羟基,故F为 ,由F与G分子式可知,F反应取代反应生成G,核磁共振图谱显示G分子有3种不同的氢原子,应发生苯环上-OCH3的对位取代,G为
,由F与G分子式可知,F反应取代反应生成G,核磁共振图谱显示G分子有3种不同的氢原子,应发生苯环上-OCH3的对位取代,G为 ,由反应条件可知,G与E反应信息中的取代反应,故Q为
,由反应条件可知,G与E反应信息中的取代反应,故Q为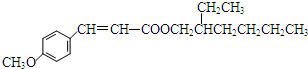 ,据此解答.
,据此解答.
解答 解:B的分子式为C3H4O,能转化得到CH2=CH-COOH,则B为CH2=CH-CHO,A为CH3CH=CH2.C8H17OH分子中只有一个支链,且为乙基,其连续氧化的产物能与NaHCO3反应生成CO2,分子中存在-CH2OH结构,其消去产物的分子中只有一个碳原子上没有氢,故C8H17OH的结构简式为 ,C与C8H17OH发生酯化反应生成D为
,C与C8H17OH发生酯化反应生成D为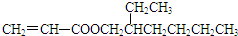 ,由E的分子式可知E为苯,F不能与NaOH溶液反应,不含酚羟基,故F为
,由E的分子式可知E为苯,F不能与NaOH溶液反应,不含酚羟基,故F为 ,由F与G分子式可知,F反应取代反应生成G,核磁共振图谱显示G分子有3种不同的氢原子,应发生苯环上-OCH3的对位取代,G为
,由F与G分子式可知,F反应取代反应生成G,核磁共振图谱显示G分子有3种不同的氢原子,应发生苯环上-OCH3的对位取代,G为 ,由反应条件可知,G与E反应信息中的取代反应,故Q为
,由反应条件可知,G与E反应信息中的取代反应,故Q为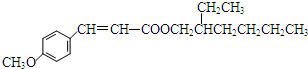 .
.
(1)反应⑤的反应类型为取代反应,G的结构简式为 ,
,
故答案为:取代反应; ;
;
(2)C中官能团的名称是:羧基、碳碳双键,C8H17OH的结构简式为 ,C8H17OH的名称(用系统命名法命名)为:2-乙基-1-己醇,
,C8H17OH的名称(用系统命名法命名)为:2-乙基-1-己醇,
故答案为:羧基、碳碳双键;2-乙基-1-己醇;
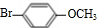
(3)X是F( )的同分异构体,X遇氯化铁溶液发生显色反应,说明含有酚羟基,且环上的一溴取代物有两种,甲基与酚羟基处于对位,X的结构简式:
)的同分异构体,X遇氯化铁溶液发生显色反应,说明含有酚羟基,且环上的一溴取代物有两种,甲基与酚羟基处于对位,X的结构简式: ,
,
故答案为: ;
;
(4)B为CH2=CH-CHO,C为CH2=CH-COOH,
a.二者均含有碳碳双键,且B还含有醛基,都能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色,故a正确;
b.B中没有羧基,不能与碳酸氢钠溶液反应产生二氧化碳,故b错误;
c.C中只有碳碳双键能与氢气发生加成反应,1mol消耗1mol氢气,标况下消耗氢气体积为22.4L,故c错误;
d.B中含有醛基,能与新制氢氧化铜悬浊液发生氧化反应,C中含有羧基,能与氢氧化铜发生中和反应,故d正确.
故选:ad;
(5)分离提纯中间产物D的操作:先用饱和碳酸钠溶液除去C和浓硫酸,再用水洗涤,弃去水层,最终通过蒸馏操作除去C8H17OH,精制得到D,
故答案为:蒸馏;
(6)反应⑥的化学方程式: +
+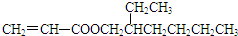 $→_{Na_{2}CO_{3}/NMP}^{Pd/C}$
$→_{Na_{2}CO_{3}/NMP}^{Pd/C}$ 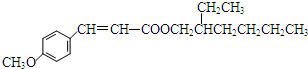 +HBr,
+HBr,
故答案为: +
+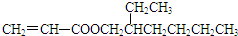 $→_{Na_{2}CO_{3}/NMP}^{Pd/C}$
$→_{Na_{2}CO_{3}/NMP}^{Pd/C}$ 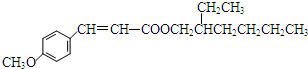 +HBr.
+HBr.
点评 本题考查有机物的推断与合成,难度中等,充分利用分子式及题目信息中物质性质、结构特点进行推理判断,熟练掌握官能团的性质与演变,侧重考查学生分析推理能力.


科目:高中化学 来源: 题型:选择题
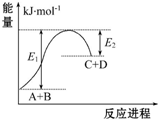
| A. | 该反应为放热反应 | |
| B. | 该反应吸收的能量为(E1-E2) | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | 该反应只有在加热条件下才能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;反应类型为:酯化反应(取代反应).
;反应类型为:酯化反应(取代反应). .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com