
分析 (1)Na2S与Na3[Ag(S2O3)2]发生的是复分解反应;
(2)求出2L废定影液中含有的银的物质的量,然后根据2molAg~2molNa3[Ag(S2O3)2]~1molNa2S来计算.
解答 解:(1)Na2S与Na3[Ag(S2O3)2]发生的是复分解反应,除了生成Ag2S沉淀还生成Na2S2O3,化学方程式为:Na2S+2Na3[Ag(S2O3)2]=Ag2S↓+4Na2S2O3;故答案为:Na2S+2Na3[Ag(S2O3)2]=Ag2S↓+4Na2S2O3;
(2)2L废定影液中含有的银的质量为m=5.68g/L×2L=11.36g,物质的量n=$\frac{11.36g}{108g/mol}$=0.1052mol,设Na2S的物质的量为xmol,根据2molAg~2molNa3[Ag(S2O3)2]~1molNa2S可有:
2molAg~2molNa3[Ag(S2O3)2]~1molNa2S
2 1
0.1052mol xmol
则有:$\frac{2}{0.1052mol}=\frac{1}{xmol}$
解得x=0.0526mol
故答案为:0.0526mol.
点评 本题依托滴定的有关知识,迁移考查了化学方程式的书写和有关计算,理清反应原理是解题关键,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
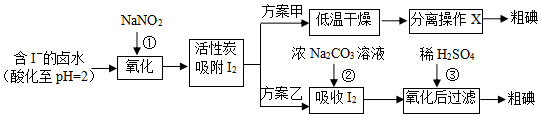
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、C1-、CO32-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol•L-1 | B. | 2 mol•L-1 | C. | 4 mol•L-1 | D. | 5 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com