


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
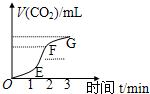
| A����ʯ��ʯ������ϸ�������ᷴӦ |
| B��ʳƷ���ڱ��������� |
| C����MnO2��H2O2�ֽⷴӦ�Ĵ��� |
| D�������ռ���Һ��Ӧʱ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��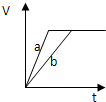 | B��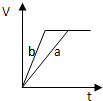 | C��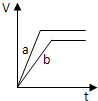 | D��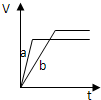 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ |
| B������ϡ���ᣬ����98%��Ũ���� |
| C���μ�����CuSO4��Һ |
| D��������Ƭ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ʵ�� | Ӱ�����ʵ����� |
| ����ʳ���ױ��� | ______ |
| ���������б��ڿ�����ȼ�տ� | ______ |
| ��״��̼��������ᷴӦ�ȿ�״��̼��Ʒ�Ӧ�� | ______ |
| �������������̻�Ϲ��ȿɿ��ٲ������� | ______ |
| ��ҵ�ϳɰ�ͨ��Ҫ�ڸ�ѹ�½��� | ______ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��������ĩ�� ���ͣ������
 CO2(g)+H2(g) ���ܱ������У���1.0 mol CO��1.0mol
CO2(g)+H2(g) ���ܱ������У���1.0 mol CO��1.0mol 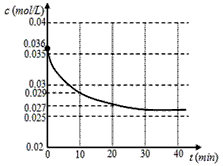
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��0101 ������ ���ͣ���ѡ��
 pC(g)+ g D(g)��v �� tͼ������ͼa���������������䣬ֻ�ڷ�Ӧǰ������ʵĴ���������v��tͼ������ͼb�� �������жϣ�
pC(g)+ g D(g)��v �� tͼ������ͼa���������������䣬ֻ�ڷ�Ӧǰ������ʵĴ���������v��tͼ������ͼb�� �������жϣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ͬ���� ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com