
�û�ѧ��Ӧԭ�����֪ʶͬ��
I�������±���ʾ��ѧ��Ӧ�����ݹ�ϵ�ش��������⣺

��1����Ӧ���� �������"���ȡ�����Ӧ��
��2�����ݷ�Ӧ����ڿ��Ƶ���ͬ����K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ����
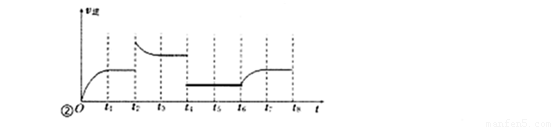
��3������Ӧ�۵��淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��

�ٷ�Ӧ��t1��t3��t7ʱ���ﵽ��ƽ�⣬��t2ʱֻ�ı���һ���������j���жϣ��ı������������ ��
����t4ʱ��ѹ��t6ʱ����Ӧ���Ũ�ȣ�����ͼ�л���t4��t6ʱ�淴Ӧ������ʱ��Ĺ�ϵ���ߡ�
II������ݴ���ĵ���ƽ��ش��������⣺
��1�������£�0.1mol��L ��CH3COOH��Һ����l����CH3COOH���ӷ������룬����Һ��pH= ��
��2����������Һ������ˮϡ�ͣ���ϡ�����У����и������������ ������ĸ��ţ���

��3��25��ʱ��CH3COOH�ĵ���ƽ�ⳣ��Ϊ1��75��10-5���ֽ�һ������CH3COOH��NaOH��Һ��ϣ�����û��ҺpH=5��6������Һ�и�����Ũ���ɴ�С��˳���� ��
��
��1������
K2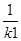
�������¶Ȼ�����CO2��Ũ�ȣ�����H2��Ũ�ȣ�
��
��1��3
��2��BD
��3�� c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
��������
�����������1�������¶ȣ�ƽ�ⳣ����������Ӧ�����ȷ�Ӧ��
K3=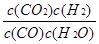 ��K1=
��K1=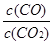 ��K2=
��K2=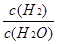 ��K3=K2X
��K3=K2X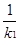
��3�������¶Ȼ�����CO2��Ũ�ȣ�����H2��Ũ�ȣ�
��1������c��H+��=c(HAc)��,��c(H+)=0.1X1%,PH=3
���볣�����䣬c(H+)��ϡ�����������Ǽ�С�ģ�ˮ�����ӻ��������䣻c(H+)��С����c(OH-)����ѡBD��
��3�������⣬�����Һ��PHΪ5.6����Һ�������ԣ����� c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
���㣺��ѧƽ��͵���ƽ�⡣���컯ѧƽ���Ӱ�������Լ�����ƽ���Ӱ�����ء�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�����ʡ���и�����ҵ��ڶ������������ۣ���ѧ���� ���ͣ������
�о���ѧ��Ӧԭ������������������壬���û�ѧ��Ӧԭ�������֪ʶ�ش��������⣺

��1����Ǧ���ص��ס����������е���Һ����֪Ǧ���ص��ܷ�ӦΪ��Pb��s����PbO2��s����2H2SO4��aq�� 2PbSO4��s����2H2O��1�������һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬����˵����ȷ����____________
2PbSO4��s����2H2O��1�������һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬����˵����ȷ����____________
����д��ţ�
A��d������
B�������ü׳ؾ���ͭ��b��ӦΪ��ͭ
C���ŵ�ʱǦ���ظ����ĵ缫��ӦʽΪ��
PbO2��s����4H����aq���� ��aq����4e��
��aq����4e�� PbSO4��s����2H2O��1��
PbSO4��s����2H2O��1��
D�����ĸ��缫���Ͼ�Ϊʯī��������6��4g Cuʱ�������й���������3��36L����
״���£�
��2��ij��Ԫ��H2A��ˮ�еĵ��뷽��ʽ�ǣ�H2A��H����HA����HA�� H����A2������ش��������⣺
H����A2������ش��������⣺
��Na2A��Һ��_________������ԡ��������ԡ����ԡ�����������________________
�������ӷ���ʽ��ʾ����
����֪0��1mol��L��1��NaHA��Һ��pH��2����0��1mol��L��1��H2A��Һ�������ӵ����ʵ���Ũ�ȿ�����__________0��1lmol��L��1���<������>���������������ǣ�___________________________.
��3����������һ����Ҫ�����ȼ�ϣ�����ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g����CO��g�� CH3OH��g���� ��H����90��8kJ��mol��1
CH3OH��g���� ��H����90��8kJ��mol��1
��2CH3OH��g�� CH3OCH3��g����H2O��g����
��H����23��5kJ��mol��1
CH3OCH3��g����H2O��g����
��H����23��5kJ��mol��1
��CO��g����H2O��g�� CO2��g����H2��g����������41��3kJ��mol��1
CO2��g����H2��g����������41��3kJ��mol��1
д��ˮú��ֱ�Ӻϳɶ�����ͬʱ����CO2���Ȼ�ѧ��Ӧ����ʽ___________________.
��4��SO2��������������Ҫ�м���Ҳ�ǿ�����Ⱦ����Ҫԭ��֮һ������������SO3�ķ�ӦΪ��2SO2��g����O2��g�� 2SO3��g������һ���¶��£���0��23 mol
SO2��0��11 mol���������ݻ�Ϊl L���ܱ������з�����Ӧ���ﵽƽ���õ�0��12 mol SO3����Ӧ��ƽ�ⳣ��K��________�����¶Ȳ��䣬�ټ���0��50
mol���������´ﵽƽ�⣬��SO3�����������___________������������䡱��С������
2SO3��g������һ���¶��£���0��23 mol
SO2��0��11 mol���������ݻ�Ϊl L���ܱ������з�����Ӧ���ﵽƽ���õ�0��12 mol SO3����Ӧ��ƽ�ⳣ��K��________�����¶Ȳ��䣬�ټ���0��50
mol���������´ﵽƽ�⣬��SO3�����������___________������������䡱��С������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡģ���� ���ͣ������
 CH3OH(g) ��H1����116 kJ/mol
CH3OH(g) ��H1����116 kJ/mol ��H2����283 kJ��mol-1
��H2����283 kJ��mol-1  ��H3����242 kJ��mol-1
��H3����242 kJ��mol-1 
 CH3OH(g) ��ƽ�ⳣ��K =__________��
CH3OH(g) ��ƽ�ⳣ��K =__________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������ ���ͣ������
 CH3OH(g) ��H1����116 kJ/mol
CH3OH(g) ��H1����116 kJ/mol ��H2����283 kJ��mol-1
��H2����283 kJ��mol-1  ��H3����242 kJ��mol-1
��H3����242 kJ��mol-1 
 CH3OH(g) ��ƽ�ⳣ��K =__________��
CH3OH(g) ��ƽ�ⳣ��K =__________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡģ���� ���ͣ������
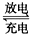 2PbSO4(s) +2H2O(l)�����һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬����˵����ȷ����____________����д��ţ���
2PbSO4(s) +2H2O(l)�����һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬����˵����ȷ����____________����д��ţ��� 
 H++A2-��
H++A2-��  CH3OH(g) ��H=-90.8kJ/mol
CH3OH(g) ��H=-90.8kJ/mol  CH3OCH3(g)+H2O(g) ��H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) ��H=-23.5kJ/mol  CO2(g)+H2(g) ��H=-41.3kJ/mol
CO2(g)+H2(g) ��H=-41.3kJ/mol  2SO3(g)����һ���¶��£���0.23molSO2��0.11molO2ͨ���ݻ�Ϊ1L���ܱ������з�����Ӧ���ﵽƽ���õ�0.12molSO3����Ӧ��ƽ�ⳣ��K=__________�����¶Ȳ��䣬��ͨ��0.50molO2�����´ﵽƽ�⣬��SO3�����������__________����������䡱��С������
2SO3(g)����һ���¶��£���0.23molSO2��0.11molO2ͨ���ݻ�Ϊ1L���ܱ������з�����Ӧ���ﵽƽ���õ�0.12molSO3����Ӧ��ƽ�ⳣ��K=__________�����¶Ȳ��䣬��ͨ��0.50molO2�����´ﵽƽ�⣬��SO3�����������__________����������䡱��С������ �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�о���ѧ��Ӧԭ������������������壬���û�ѧ��Ӧԭ�������֪ʶ�ش��������⣺
��1����Ǧ���ص��ס����������е���Һ����֪Ǧ���ص��ܷ�ӦΪ��Pb��s����PbO2��s����2H2SO4��aq��2PbSO4��s����2H2O��1�������һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬����˵����ȷ����____________
����д��ţ�
A��d������
B�������ü׳ؾ���ͭ��b��ӦΪ��ͭ
C���ŵ�ʱǦ���ظ����ĵ缫��ӦʽΪ��
PbO2��s����4H����aq������aq����4e��
PbSO4��s����2H2O��1��
D�����ĸ��缫���Ͼ�Ϊʯī��������6��4g Cuʱ�������й���������3��36L����
״���£�
��2��ij��Ԫ��H2A��ˮ�еĵ��뷽��ʽ�ǣ�H2A��H����HA����HA��H����A2������ش��������⣺
��Na2A��Һ��_________������ԡ��������ԡ����ԡ�����������________________
�������ӷ���ʽ��ʾ����
����֪0��1mol��L��1��NaHA��Һ��pH��2����0��1mol��L��1��H2A��Һ�������ӵ����ʵ���Ũ�ȿ�����__________0��1lmol��L��1���<������>���������������ǣ�___________________________.
��3����������һ����Ҫ�����ȼ�ϣ�����ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g����CO��g��CH3OH��g���� ��H����90��8kJ��mol��1
��2CH3OH��g��CH3OCH3��g����H2O��g������H����23��5kJ��mol��1
��CO��g����H2O��g��CO2��g����H2��g����������41��3kJ��mol��1
д��ˮú��ֱ�Ӻϳɶ�����ͬʱ����CO2���Ȼ�ѧ��Ӧ����ʽ___________________.
��4��SO2��������������Ҫ�м���Ҳ�ǿ�����Ⱦ����Ҫԭ��֮һ������������SO3�ķ�ӦΪ��2SO2��g����O2��g��2SO3��g������һ���¶��£���0��23 molSO2��0��11 mol���������ݻ�Ϊl L���ܱ������з�����Ӧ���ﵽƽ���õ�0��12 mol SO3����Ӧ��ƽ�ⳣ��K��________�����¶Ȳ��䣬�ټ���0��50mol���������´ﵽƽ�⣬��SO3�����������___________������������䡱��С������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com