
����Ŀ���о�PM 2.5��SO2��NOx�ȣ��Լ���������������Ҫ���壮ȡij����������ˮ�����Ƴɴ���Һ�������������ӵĻ�ѧ��ּ���Ũ�����±���
���� | K+ | Na+ | NH4+ | H+ | SO42�� | NO3�� | Cl�� |
Ũ��/molL��1 | 4��10��6 | 6��10��6 | 2��10��5 | a | 4��10��5 | 3��10��5 | 2��10��5 |
��ش��������⣺
��1�����ݱ������ݼ���˴���Һ��c��H+��Ũ��aΪmol/L��
��2��NOx������β���е���Ҫ��Ⱦ��֮һ�� ����������������ʱ�ĸ��»�����N2��O2��Ӧ����Ӧ�Ļ�ѧ����ʽ�� ��
��NOx���γ����꣬��NO2�γ��������Ҫ��Ӧ����д���ӷ���ʽ����
��3��Ϊ����SO2���ŷţ�����ȡ�Ĵ�ʩ�У� ����ȼú�м�����ʯ�ҿ�����������ã�SO2�����պ�ת����һ����Ԫ�ص����̬�Ļ���������ʵĻ�ѧʽ�� ��
�����������е�SO2 �� �������ʿ������ռ�����������ţ������Ṥҵ�е�β��SO2����ѭ�����ã�д��SO2ת��ΪSO3��Ӧ�Ļ�ѧ����ʽ �� a��NaOH b��H2SO4 c��NaHSO3 ��
���𰸡�
��1��1��10��4
��2��N2+O2 ![]() 2NO��3NO2+H2O�T2H++2NO3��+NO
2NO��3NO2+H2O�T2H++2NO3��+NO
��3��CaSO4��a��2SO2+O2 ![]() 2SO3
2SO3
���������⣺��1����Һ�д��ڵ���غ�c��K+��+c��Na+��+c��NH4+��+c��H+��=2c��SO42����+c��NO3����+c��Cl�������ͼ�����ݼ���õ�������Ũ��c��H+��=1��10��4 mol/L�� ���Դ��ǣ�1��10��4 ����2������������������ʱ�ĸ��»�����N2��O2��Ӧ����Ӧ�Ļ�ѧ����ʽ��N2+O2 ![]() 2NO��
2NO��
���Դ��ǣ�N2+O2 ![]() 2NO����NOx���γ����꣬��NO2�γɵ�����Ϊ���������꣬������Һ�к��е���Ҫ������H+��NO3�� �� ��Ӧ�����ӷ���ʽΪ��3NO2+H2O�T2H++2NO3��+NO��
2NO����NOx���γ����꣬��NO2�γɵ�����Ϊ���������꣬������Һ�к��е���Ҫ������H+��NO3�� �� ��Ӧ�����ӷ���ʽΪ��3NO2+H2O�T2H++2NO3��+NO��
���Դ��ǣ�3NO2+H2O�T2H++2NO3��+NO����3������ȼú�м�����ʯ�ҿ�����������ã�SO2�����պ�ת����һ����Ԫ�ص����̬�Ļ�����������ƺͶ�������Ӧ����������ƣ�������Ʊ��������ΰ����ƣ�CaO+SO2+O2=CaSO4 �� ���̬�Ļ�����ΪCaSO4 ��
���Դ��ǣ�CaSO4���ڶ������������������
a������������Һ�������ն��������������������ƻ��������ƣ���a��ȷ��
b����������ն�������b����
c��NaHSO3�������ն�������c����
��ѡa��
���Ṥҵ�е�β��SO2����ѭ�����ã�д��SO2ת��ΪSO3��Ӧ�Ļ�ѧ����ʽΪ��2SO2+O2 ![]() 2SO3 ��
2SO3 ��
���Դ��ǣ�a��2SO2+O2 ![]() 2SO3 ��
2SO3 ��
�����㾫����������Ҫ�����˶����������Ⱦ�����������֪ʶ�㣬��Ҫ����SO2����Ⱦ��������Ҫ�к�����֮һ��ֱ��Σ��������������������γ�����pH��5��6���ƻ�ũ���ɭ�֡���ԭ��ʹ����������ǿ�ȵȣ���SO2�Ĺ�ҵ�������뾭���������������ŷŵ������в�����ȷ�����⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��A��ͨ�����Cl2 �� �ر�B��ʱ��C���ĺ�ɫ������������������B����C����ɫ��������ɫ����Dƿ��װ���ǣ� �� 
A.ŨH2SO4
B.NaOH��Һ
C.Ũ����
D.����NaCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���Ľṹ��ʾ����ȷ���ǣ� ��
A.CH4�����ģ��ʾ��ͼΪ�� ![]()
B.��ϩ��ʵ��ʽΪ��CH2
C.�Ҵ��Ľṹ��ʽ��C2H5OH
D.2���һ���1��3������ϩ���ӵļ���ʽ�� ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֦������������о�����ṹ��ʽ��ͼ�����й��ڷ�֦���������ȷ���ǣ� �� 
A.�����Ҵ������ᷴӦ���ҷ�Ӧ������ͬ
B.�����к���3�ֹ�����
C.1mol��֦��������3molNaOH�����кͷ�Ӧ
D.��ʹ������Ȼ�̼��Һ�����Ը��������Һ��ɫ����ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ���������CO2�ĺ�����������⣬ij��ѧ���������ɫ���ɡ����룺�ѹ����ų��ĸ���CO2�ķ�������������̼�����Һ���գ�Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧʹ�����е�CO2ת��Ϊȼ�ϼ״�������ɫ���ɡ�����IJ��ּ���������ͼ1 
��1���ϳ����з�Ӧ�Ļ�ѧ����ʽΪ����H��0����ƽ���ƶ�ԭ���������������������ԭ������ƽ��ת���ʣ���ʵ�������в���300����¶ȣ��������¶ȶԷ�Ӧ���ʵ�Ӱ���⣬����Ҫ������ ��
��2���Ӻϳ���������״���ԭ�������в�����ԭ���Ƚ����������ĸ��
A.����
B.��Һ
C.����
D.�ᾧ
��3�������Ϊ2L�ĺϳ����У�����2mol CO2��6mol H2 �� ���CO2��g����CH3OH��g����Ũ����ʱ��仯��ͼ2��ʾ�� �ӷ�Ӧ��ʼ��ƽ�⣬V��H2��=����ʹƽ����ϵ�� ![]() ����Ĵ�ʩ�� ��
����Ĵ�ʩ�� ��
��4���罫CO2��H2��1��4������Ȼ�ϣ����ʵ��������¿��Ƶ�CH4 �� ��֪
CH4��g��+2O2��g���TCO2��g��+2H2O��l����H1=��890.3kJ/mol
H2��g��+ ![]() O2��g���TH2O��l����H2=��285.5kJ/mol
O2��g���TH2O��l����H2=��285.5kJ/mol
д��CO2��g����H2��g����Ӧ����CH4��g����Һ̬ˮ���Ȼ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���Ľṹ��ʽ��ͼ������л���ɷ����ķ�Ӧ�����У� �� 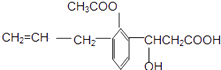
��ȡ�� �ڼӳ� ����ȥ ������ ��ˮ������� ���кͣ�
A.�٢ڢۢݢ�
B.�ڢۢܢݢ�
C.�٢ڢۢܢݢ�
D.�٢ڢۢܢݢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� ![]() ת��Ϊ
ת��Ϊ ![]() �ķ���Ϊ�� ��
�ķ���Ϊ�� ��
A.��Һ���ȣ�ͨ��������HCl
B.��������NaOH��Һ���Ⱥ���ͨ��CO2
C.��ϡH2SO4���Ⱥ���������Na2CO3
D.��ϡH2SO4���Ⱥ���������NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ���Ҵ���ȡ����ͨ������������;����
a��CH3CH2OH��g��+H2O��g��=4H2��g��+2CO��g����H1=+256.6kJmol��1
b��2CH3CH2OH��g��+O2��g��=6H2��g��+4CO��g����H2=+27.6kJmol��1
������˵����ȷ���ǣ� ��
A.����a�ķ�Ӧ�¶ȣ��Ҵ���ת��������
B.��b��֪���Ҵ���ȼ����Ϊ13.8 kJmol��1
C.2H2��g��+O2��g��=2H2O��g����H=+485.6 kJmol��1
D.��ȡ������������;��b���ĵ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У������ʡ������������˳��������ȷ����
A��ϡ�����塢���ء���ˮ�����
B���Ҵ���Ũ���ᡢ����
C�����ʯ������ʯ������ʯ
D��ˮ����ˮ������ˮú��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com