
| A£® | p£ØNe£©£¾p£ØN2£©£¾p£ØO2£© | B£® | p£ØO2£©£¾p£ØNe£©£¾p£ØN2£© | C£® | p£ØN2£©£¾p£ØO2£©£¾p£ØNe£© | D£® | p£ØN2£©£¾p£ØNe£©£¾p£ØO2£© |
·ÖĪö ŌŚĪĀ¶ČŗĶĆܶȶ¼ĻąĶ¬Ģõ¼žĻĀ£¬ČēĢå»żĻąĶ¬£¬ŌņÖŹĮæĻąĶ¬£¬ĘųĢåµÄĪļÖŹµÄĮæŌ½“ó£¬Ń¹ĒæŌ½“ó£¬Ń¹ĒæÓėĦ¶ūÖŹĮæ³É·“±Č£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗŌŚĪĀ¶ČŗĶĆܶȶ¼ĻąĶ¬Ģõ¼žĻĀ£¬ČēĢå»żĻąĶ¬£¬ŌņÖŹĮæĻąĶ¬£¬ĘųĢåµÄĪļÖŹµÄĮæŌ½“ó£¬Ń¹ĒæŌ½“ó£¬Ń¹ĒæÓėĦ¶ūÖŹĮæ³É·“±Č£¬
Ħ¶ūÖŹĮæNe£¼N2£¼O2£¬Ń¹Ēæ£Øp£©“ӓ󵽊”µÄĖ³ŠņĪŖp£ØNe£©£¾p£ØN2£©£¾p£ØO2£©£¬Ń”ĻīÖŠÖ»ÓŠA·ūŗĻ£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°¢·üŁ¤µĀĀŽ¶ØĀɼ°ĶĘĀŪ£¬Ķ¬Ź±æ¼²éѧɜ·ÖĪöĪŹĢā”¢½ā¾öĪŹĢāÄÜĮ¦£¬×¢Ņā°ŃĪÕ±Č½ĻŃ¹Ēæ“󊔵ĽĒ¶ČŗĶĻą¹Ų¼ĘĖć¹«Ź½µÄŌĖÓĆ£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģįøß³ōŃõÅضČŅŌøÄÉĘæÕĘųÖŹĮæ | B£® | ĢįÉżæóĪļČ¼ĮĻµÄĶŃĮņĶŃĻõ¼¼Źõ | ||
| C£® | ŃŠ·¢Ģ«ŃōÄÜĘū³µ“śĢęČ¼ÓĶĘū³µ | D£® | æŖ·¢²»ŗ¬µŖ”¢Į×µÄĻ“µÓĒå½ą¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
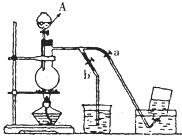 ČēĶ¼±ķŹ¾ŌŚĆ»ÓŠĶØ·ē³÷µÄĢõ¼žĻĀÖʱøĀČĘųŹ±µÄ×°ÖĆ£¬Ķ¼ÖŠa”¢bŹĒæÉæŲÖĘµÄµÆ»ÉĢś¼Š£®£ØŅŃÖŖ£ŗĀČĘųŌŚ±„ŗĶĀČ»ÆÄĘČÜŅŗÖŠµÄČܽā¶Č½ĻŠ”£®
ČēĶ¼±ķŹ¾ŌŚĆ»ÓŠĶØ·ē³÷µÄĢõ¼žĻĀÖʱøĀČĘųŹ±µÄ×°ÖĆ£¬Ķ¼ÖŠa”¢bŹĒæÉæŲÖĘµÄµÆ»ÉĢś¼Š£®£ØŅŃÖŖ£ŗĀČĘųŌŚ±„ŗĶĀČ»ÆÄĘČÜŅŗÖŠµÄČܽā¶Č½ĻŠ”£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 2NH3£®
2NH3£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
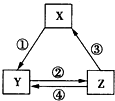 ĻĀ±ķÖŠø÷×éĪļÖŹÖ®¼äĶعżŅ»²½·“Ó¦²»æÉÄÜŹµĻÖČēĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµµÄŹĒ£Ø””””£©
ĻĀ±ķÖŠø÷×éĪļÖŹÖ®¼äĶعżŅ»²½·“Ó¦²»æÉÄÜŹµĻÖČēĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµµÄŹĒ£Ø””””£©| Ń”Ļī | X | Y | Z |
| A | Mg | MgO | MgCl2 |
| B | Fe | FeCl3 | FeCl2 |
| C | Na2CO3 | NaOH | NaHCO3 |
| D | Cl2 | Ca£ØClO£©2 | HClO |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ1£ŗ2 | B£® | 2£ŗ1£ŗ1 | C£® | 1£ŗ2£»1 | D£® | 2£ŗ2£»1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeCl2£ØFeCl3£© | B£® | KCl£ØNaCl£© | C£® | Fe2O3£ØAl2O3£© | D£® | NaCl£ØMgCl2£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
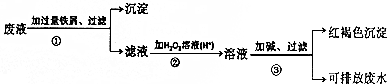
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com