
| A、强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
| B、溶液中导电能力的强弱主要与溶液中的离子浓度大小和离子所带电荷数有关 |
| C、强弱电解质的本质区别是溶液导电能力的强弱 |
| D、强电解质的溶液中只有离子,没有分子存在 |


科目:高中化学 来源: 题型:
| A、0.1L该溶液中含有NaOH 4.0g |
| B、从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol?L-1 |
| C、100 mL该溶液中含有OH-0.01mol |
| D、在1 L水中溶解4g NaOH即可配制得0.1 mol?L-1NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 产生气体 | 无气体 |
解释 | CO32-+H+?HCO3- | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
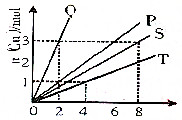 铜和硝酸反应的物质的量的关系如图所示,纵坐标表示消耗铜的物质的量,横坐标表示消耗硝酸的物质的量,坐标图中各条线表示下列反应:
铜和硝酸反应的物质的量的关系如图所示,纵坐标表示消耗铜的物质的量,横坐标表示消耗硝酸的物质的量,坐标图中各条线表示下列反应:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(CH3COO-)>c(H+)>c(Na+ )>c(OH-) |
| B、c(Na+ )>c(OH-)>c(CH3COO-)>c(H+ ) |
| C、c(OH-)>c(Na+ )>c(H+ )>c(CH3COO-) |
| D、c(Na+ )>c(CH3COO-)>c(OH-)>c(H+ ) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) |
| B、若用50 mL 0.55 mol?L-1的氢氧化钠溶液,分别与50 mL 0.50 mol?L-1的盐酸和50 mL0.50mol?L-1硫酸充分反应,两反应的中和热不相等 |
| C、0.2 mol/L HCl溶液与等体积0.05 mol/L Ba(OH)2 溶液混合后,溶液的pH=1 |
| D、0.2 mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=2c(CO32-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下pH=7的溶液中:Fe3+、Na+、Cl-、SCN- |
| B、常温下c(OH-)/c(H+)=1014的溶液中:K+、Mg2+、Cl-、Br- |
| C、含有大量HCO3-的澄清透明溶液中:K+、C6H5O-、Cl-、Na+ |
| D、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | ① | ② | ③ | 实验结论 | 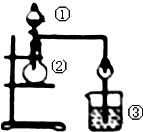 |
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:C>Si |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com