


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
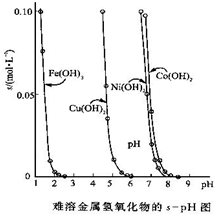 金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的.难溶金属的氢氧化物在不同pH下的溶解度(s,mol?L-1)如图.
金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的.难溶金属的氢氧化物在不同pH下的溶解度(s,mol?L-1)如图.| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将某钾盐溶于盐酸后产生能使澄清石灰水变浑浊的无色无味的气体 | 说明该钾盐是K2CO3 |
| B | 向含有少量FeCl3的CuCl2溶液中加入足量Cu粉,搅拌一段时间后过滤 | 除去CuCl2溶液中的少量FeCl3,提纯CuCl2溶液 |
| C | 常温下,向饱和Na2CO3溶液中通入过量CO2,溶液变浑浊 | 说明常温下NaHCO3的溶解度可能比Na2CO3的溶解度小 |
| D | C2H5OH与浓硫酸在170℃共热,将制得的气体直接通入酸性KMnO4溶液中 | 检验制得气体是否为乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| [CO] | [CO2] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com