
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A、向醋酸溶液加水稀释时,醋酸的电离平衡逆向移动 |
| B、等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| C、a mol/L HCN溶液与b mol/L NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
| D、同浓度CH3COONa和KCN溶液中c(Na+)-c(CH3COO-)小于的c(K+)-c(CN-) |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化还原反应中,某元素由化合态变为游离态时,一定被还原 |
| B、阳离子只有氧化性,阴离子只有还原性 |
| C、氧化剂在氧化还原反应中,本身被还原 |
| D、氧化还原反应的实质是化合价的升降 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C、HCO3-的水解程度大于HCO3-的电离程度 |
| D、c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.5×10-4 |
| B、0.015 |
| C、5.4×10-5 |
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.24L |
| B、1.12L |
| C、0.56L |
| D、0.28L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | A | B | C | D |
| 实验 |  |  |  |  |
| 结论 | 能组成Zn-Cu原电池 | 实验室制取少量的乙酸乙酯 | 白色沉淀 为BaSO3 | 用氯化钠与浓硫酸制取(可加热)、净化、收集氯化氢 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
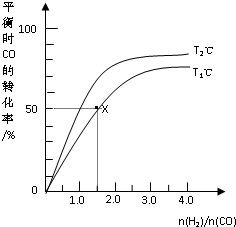 在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0.有关信息如图所示,下列说法正确的是( )
在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0.有关信息如图所示,下列说法正确的是( )| A、T1<T2 | ||
| B、T1℃时该反应的平衡常数为4.0 L2?mol-2 | ||
C、同一温度下,
| ||
D、相同条件下
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com