
磺酰氯(SO2Cl2)是一种有机氯化剂,也是锂电池正极活性物质。已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解。
(1)已知:SO2 (g) +Cl2 (g)+ SCl2 (g) 2SOCl2 (g) △H=a kJ·mol-1
2SOCl2 (g) △H=a kJ·mol-1
SO2Cl2(g)+ SCl2 (g)  2SOCl2(g) △H=b kJ·mol-1
2SOCl2(g) △H=b kJ·mol-1
则反应:SO2(g) + Cl2 (g) SO2Cl2(g) △H = ▲ kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K = ▲ 。
SO2Cl2(g) △H = ▲ kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K = ▲ 。
(2)磺酰氯可与白磷发生反应为:P4 + 10 SO2Cl2 = 4PCl5 + 10SO2↑,若生成1molSO2,则转移电子的物质的量为 ▲ mol。
(3)某学习小组的同学依据反应:SO2(g)+ Cl2(g) SO2Cl2(g) △H <0,设计的制备磺酰氯装置如题20图-1。
SO2Cl2(g) △H <0,设计的制备磺酰氯装置如题20图-1。

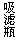

①若用浓盐酸与二氧化锰为原料制取Cl2,其反应的化学方程式为 ▲ 。
②有关题20图-1所示的装置说法正确的是 ▲ (不定项选择)。
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和Na2SO3溶液
b.B处反应管内五球中玻璃棉上的活性炭作催化剂
c.B处反应管冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
③从化学平衡移动角度分析,反应管通水冷却的目的为 ▲ 。
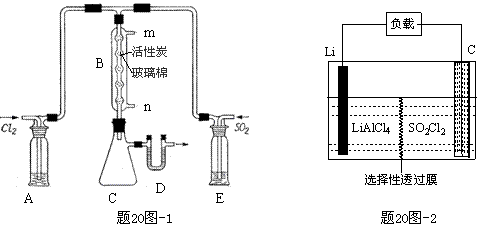
(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如题20图-2所示,已知电池反应为:
2Li + SO2Cl2 = 2LiCl + SO2↑;则电池工作时,正极的电极反应式为 ▲ 。
 互动课堂系列答案
互动课堂系列答案科目:高中化学 来源: 题型:
下列实验设计方案中,可行的是
A.用加入过量CuCl2溶液,再过滤,除去Cu(NO3)2溶液中混有的AgNO3
B.某固体在加入稀盐酸产生了无色无味且能使澄清石灰水变浑浊的气体,证明该固体一定含有CO32-
C.向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的SO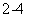





 D.先后滴加紫色石蕊试液、BaCl2溶液,可以将盐酸、硫酸氢钠、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开
D.先后滴加紫色石蕊试液、BaCl2溶液,可以将盐酸、硫酸氢钠、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开
查看答案和解析>>
科目:高中化学 来源: 题型:
.一定量的CuS和Cu2S的混合物投入足量的 HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为
HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为
A.9.0L B.13.5L C.15.7L D.16.8L
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,甲组中的某种物质能与乙组中的所有物质发生反应,甲组中的该物质是 ( )
| 甲组 | ①Al(OH)3 ②SiO2 ③ FeCl3溶液 ④ SO2 |
| 乙组 | a.NaOH溶液 b.浓HNO3 c.氨水 d.氯水 e.H2O2溶液 |
A.① B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
氮氧化物与悬浮在大气中海盐粒子的相互反应:
4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+ Cl2(g),ΔH
2NaNO3(s)+2NO(g)+ Cl2(g),ΔH
在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是 ( )
A.10min内NO浓度变化表示的速率v(NO)=0.01 mol·L-1·min-1
B.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α
C.若升高温度,平衡逆向移动,则该反应的ΔH>0
D.若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
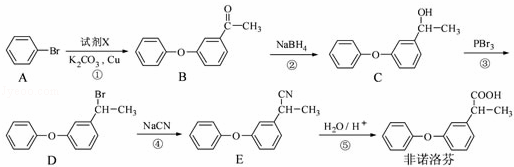
请回答下列问题:
(1)非诺洛芬中的含氧官能团为 和 (填名称).
(2)反应①中加入的试剂X的分子式为C8H8O2,X的结构简式为 .
(3)在上述五步反应中,属于取代反应的是 (填序号).
(4)B的一种同分异构体满足下列条件:
Ⅰ、能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应.
Ⅱ、分子中有6种不同化学环境的氢,且分子中含有两个苯环.
写出该同分异构体的结构简式: .
(5)根据已有知识并结合相关信息,写出以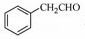 为原料制备
为原料制备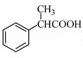 的合成路线流程图(无机试剂任用),合成路线路程图示例如下:
的合成路线流程图(无机试剂任用),合成路线路程图示例如下:
CH3CH2Br CH3CH2OH
CH3CH2OH CH3COOCH2CH3.
CH3COOCH2CH3.
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变 化如表:
化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应,在第5 s时,NO的转化率为________。
(2)如图所示,表示NO2变化曲线的是________。用O2表示从0 s~2 s内该反应的平均速率v=________________。
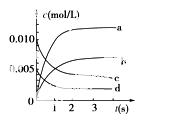
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c .v逆(NO)=2v正(O2) d.容器内密度保持不变
.v逆(NO)=2v正(O2) d.容器内密度保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com