
 CH3OH(g),甲醇生成量与时间的关系如下图所示。
CH3OH(g),甲醇生成量与时间的关系如下图所示。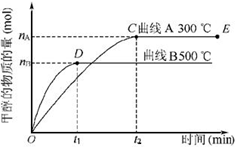
| A.在300 ℃条件下,t1时刻该反应达到化学平衡 |
| B.在500 ℃条件下,从反应开始到平衡,氢气的平均反应速率v(H2)为nB/(3t1) mol/L |
| C.在其他条件不变的情况下,将处于E点的体系体积压缩到原来的1/2,则氢气的浓度减小 |
| D.由图像说明该反应的正反应为放热反应 |
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.体系有序性越高,熵值就越低 | B.自发过程将导致体系的熵增大 |
| C.吸热反应一定不可以自发进行 | D.同种物质气态时熵值最大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+3D(g)ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同。
C(g)+3D(g)ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同。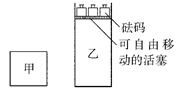
| A.甲、乙两容器中的反应达到化学平衡时,C的体积分数相等 |
| B.甲、乙两容器中的反应达到化学平衡时,两容器内压强不相等 |
| C.向甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度不变 |
| D.向乙容器中再充入2molC和6molD,平衡后乙中物质C的浓度为原来的2倍 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+D(g),当下列物理量不发生变化时:①混合气体的密度②容器内气体的压强③混合气体的平均相对分子质量④B的物质的量浓度 能表明该反应一定已达到平衡状态的是( )
C(g)+D(g),当下列物理量不发生变化时:①混合气体的密度②容器内气体的压强③混合气体的平均相对分子质量④B的物质的量浓度 能表明该反应一定已达到平衡状态的是( )| A.①③④ | B.②③ | C.②③④ | D.只有④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.达到平衡后,降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数 |
| B.达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动 |
| C.达到平衡时,反应速率v正(X)=2v逆(Z) |
| D.平衡常数K值越大,X的转化率越大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 3KCl + Fe(SCN)3,达到平衡后溶液显红色,能使平衡逆向移动的条件是
3KCl + Fe(SCN)3,达到平衡后溶液显红色,能使平衡逆向移动的条件是| A.向溶液中加少量KCl晶体 | B.向溶液中加入少量水 |
| C.向溶液中滴入数滴 1mol/L FeCl3 | D.设法移走部分水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g)+H2(g) △H<0 试回答下列问题:
CO2(g)+H2(g) △H<0 试回答下列问题: -1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=
-1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=  大于”、“小于”或“等于”)。
大于”、“小于”或“等于”)。 大”、“减小”或“不变”),
大”、“减小”或“不变”),查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等于8 mol | B.等于1.6 mol | C.大于0.8 mol小于1.6 mol? | D.大于1.6 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
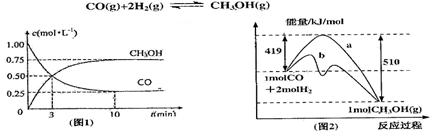
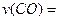 ;
;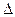 H>0”)反应,写出反应的热化学方程式 ;选择适宜的催化剂, (填“能”或“不能”)改变该反应的反应热;
H>0”)反应,写出反应的热化学方程式 ;选择适宜的催化剂, (填“能”或“不能”)改变该反应的反应热; 达式为 ,温度升高,平衡常数K (填“增大”、“不变”或“减小”);
达式为 ,温度升高,平衡常数K (填“增大”、“不变”或“减小”);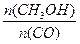 增大的 。
增大的 。 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com