
下列有关元素的性质及其递变规律正确的是 ( )
A.ⅠA族与 ⅦA族元素间可形成共价化合物或离子化合物
ⅦA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性越强,水解程度越大
D.同周期金属元素的化合价越高,其原子失电子能力越强
科目:高中化学 来源: 题型:
实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:

(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为 ;该操作将I2还原为I-的目的是 。
 (4)已知:5SO32—+2IO3—+2H+
(4)已知:5SO32—+2IO3—+2H+ I2+5SO42—+H2O
I2+5SO42—+H2O
某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3—中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3—的实验方案:取适量 含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在; 。
含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在; 。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B 在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是 ,写出一种工业制备单质F的离子方程式 。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为 ,其水溶液与F单质反应的化学方程式为 ;在产物中加入少量KI,反应后加人CC14并振荡,有 机层显 色。
(3)由这些元素组成的物质,其组成和结构信息如下表:

a的化学式为 ;b的化学式为 ;;c的电子式为 ;
d的晶体类型是 。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过 键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
若A、B是相邻周期同主族元素(A在B上一周期),A、B所在周期分别有m种和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为________________。
答案 y=x+m或y=x+n
解析 当A、B在ⅠA族和 ⅡA族时,y=x+m,当A、B在ⅢA~ⅦA族时,y=x+n。
ⅡA族时,y=x+m,当A、B在ⅢA~ⅦA族时,y=x+n。
查看答案和解析>>
科目:高中化学 来源: 题型:
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是 ( )
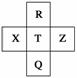
A.非金属性:Z<T<X
B.R与Q的电子数相差26
C.气态氢化物稳定性:R<T<Q
D.最高价氧化物的水化物的酸性:T<Q
查看答案和解析>>
科目:高中化学 来源: 题型:
某高校化学工作者创建了“元素立体周期律”,在原来二维周期表横列( X轴)和纵列(Y轴)基础上,增加了一个竖列(Z轴)。Z轴按“中质差”(中子数和质子数之差ΔZ=N-P)自上而下递增顺序排列。原“二维元素周期表”中的相对原子质量由同位素“中质和”(中子数和质子数之和A=N+P)替代。下列说法正确的是 ( )
X轴)和纵列(Y轴)基础上,增加了一个竖列(Z轴)。Z轴按“中质差”(中子数和质子数之差ΔZ=N-P)自上而下递增顺序排列。原“二维元素周期表”中的相对原子质量由同位素“中质和”(中子数和质子数之和A=N+P)替代。下列说法正确的是 ( )
A.“中质和”相同的核素一定是同一元素
B.“中质差”相同的核素一定是同一元素
C.N2-P2=A×ΔZ
D.至2008年,人们发现108种元素有m种同位素,说明“中质差”一定有m种
查看答案和解析>>
科目:高中化学 来源: 题型:
从南方往北方长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是 ( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com