
| A. | 10mol | B. | 0.1mol | C. | 1mol | D. | 100mol |
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg(OH)2+2 HCL═Mg CL2+2 H2O | B. | 2 NaOH+H2SO4═Na2SO4+2 H2O | ||
| C. | Ba(OH)2+H2SO4═BaSO4+2 H2O | D. | 2 HCL+Cu(OH)2═CuCL2+2 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  点燃洒精灯 | B. |  称量10.05g固体 | C. | 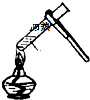 液体加热 | D. |  倾倒液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在水溶液中或熔融状态下均不导电的化合物叫非电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | NaHSO4电离时生成的阳离子有氢离子,所以是酸 | |
| D. | 纯水的导电性很差,但水不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学利用下图装置,研究氯气的性质.请据图回答:
某同学利用下图装置,研究氯气的性质.请据图回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15.5 g | B. | 15.0 g | C. | 14.5 g | D. | 16.0 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com