
 ;D的核磁共振氢谱共有3组峰.
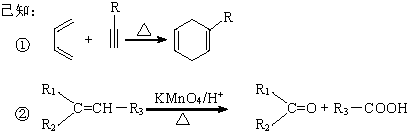
;D的核磁共振氢谱共有3组峰.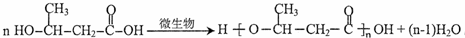 .
.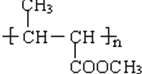
 .
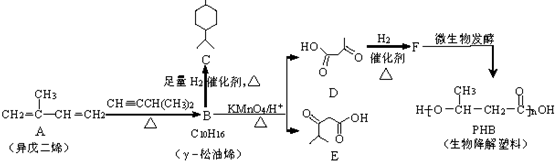
. 分析 根据题中各物转化关系,A与HC≡CCH(CH3)2 发生信息①中的加反应得B,B与氢气加成得C,根据C的结构及B的分子式可知B为 ,B发生信息②中的氧化反应得D和E,D与氢气发生加成反应得F为CH3CHOHCH2COOH,F发生缩聚反应得PHB,据此答题.
,B发生信息②中的氧化反应得D和E,D与氢气发生加成反应得F为CH3CHOHCH2COOH,F发生缩聚反应得PHB,据此答题.
解答 解:根据题中各物转化关系,A与HC≡CCH(CH3)2 发生信息①中的加反应得B,B与氢气加成得C,根据C的结构及B的分子式可知B为 ,B发生信息②中的氧化反应得D和E,D与氢气发生加成反应得F为CH3CHOHCH2COOH,F发生缩聚反应得PHB,
,B发生信息②中的氧化反应得D和E,D与氢气发生加成反应得F为CH3CHOHCH2COOH,F发生缩聚反应得PHB,
(1)根据A的结构简式可知,A的名称是2-甲基-1,3-丁二烯,B→C的反应类型是加成反应或还原反应,
故答案为:2-甲基-1,3-丁二烯;加成反应或还原反应;
(2)根据上面的分析可知,B为 ,根据D的结构简式可知,D的核磁共振氢谱共有3组峰,
,根据D的结构简式可知,D的核磁共振氢谱共有3组峰,
故答案为: ;3;
;3;
(3)上述转化关系中,D和E中所含官能团种类和数目相同,组成上相差2个CH2,所以D和E互为同系物,
故答案为:D和E;
(4)F生成PHB的化学方程式是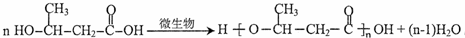 ,
,
故答案为: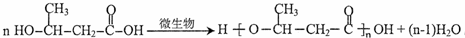 ;
;
(5)E的同分异构体中,既能发生银镜反应,即有醛基,也能与碳酸氢钠溶液反应,说明有羧基,这样的结构有OHCCH2CH2CH2CH2COOH、OHCCH2CH2CH(CH3)COOH、OHCCH2CH(CH3)CH2COOH、OHCCH(CH3)CH2CH2COOH、OHCC(CH3)2CH2COOH、OHCCH2C(CH3)2COOH、OHCCH(CH3)CH(CH3)COOH、OHCCH(CH2CH3)CH2COOH、OHCCH2CH(CH2CH3)COOH、OHCCH(CH2CH2CH3)COOH、OHCC(CH3)(CH2CH3)COOH、OHCCH(COOH)CH(CH3)2,共12种,
故答案为:12;
(6)F除了合成PHB外,还可经过消去、酯化、聚合三步反应合成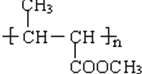 ,在催化剂作用下,第三步反应的化学方程式是
,在催化剂作用下,第三步反应的化学方程式是 ,
,
故答案为:消去; .
.
点评 本题考查有机物推断,注意根据反应条件判断发生的反应,需要学生熟练掌握官能团的性质与转化,较好的考查学生分析推理能力,难度中等.


科目:高中化学 来源: 题型:多选题
| A. | OH-+CO2→HCO3- | |
| B. | 2OH-+CO2→CO32-+H2O | |
| C. | Ca2++2OH-+CO2→CaCO3↓+H2O | |
| D. | Ca2++4OH-+2CO2→CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO和 N2为等电子体,22.4L的CO气体和1mol N2所含的电子数相等 | |
| B. | 1L密度为1.84g•cm-3质量分数为98%的硫酸溶液中,所含氢原子数为36.8NA | |
| C. | 在标准状况下,32g氧气和臭氧的混合气体中含氧原子数为2NA | |
| D. | 在标准状况下,30g福尔马林和22.4L三氧化硫所含氧原子数之比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
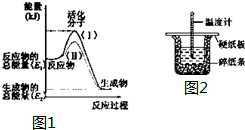 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示.请认真观察如图1,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示.请认真观察如图1,然后回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
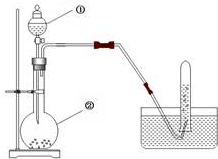 实验室用电石制取乙炔的装置如下图所示,请填空:
实验室用电石制取乙炔的装置如下图所示,请填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (3m+n)mol | B. | ($\frac{5}{2}m+\frac{n}{2}•3p$)mol | C. | (3m+n+2p)mol | D. | ($\frac{5}{2}m+\frac{n}{2}$)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向1mL 2mol•L-1 NaOH溶液加入2滴0.1mol•L-1 MgCl2溶液,再滴加2滴0.1mol•L-1 FeCl3溶液 | 先生成白色沉淀, 后生成红褐色沉淀 | Fe(OH)3比Mg(OH)2 更难溶 |
| B | 向NH3•H2O溶液中滴加少量AgNO3溶液 | 无明显现象 | NH3•H2O和AgNO3 不反应 |
| C | 向试管中某溶液加入NaOH溶液 | 试管口湿润的红色石蕊试纸不变蓝 | 溶液中无NH4+ |
| D | 浓硫酸加入Cu片后,加热 | 有白色固体生成 | 白色固体为CuSO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com