
| A.化学反应速率只能用反应物浓度的减少量表示 |
| B.只有温度和催化剂才能影响化学反应速率 |
| C.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| D.催化剂既能改变正反应的反应速率,又能改变逆反应的反应速率 |
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.②④⑥ | C.②⑤⑥ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.A为固体,C为气体,正反应为放热反应 |
| B.A、C均为气体,正反应为吸热反应 |
| C.A为气体,C为固体,正反应为吸热反应 |
| D.A为气体,C为固体,正反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3molA、2molB | 6molA、4molB | 2molC |
| 到达平衡的时间(min) | 5 | 8 | |
| A的浓度(mol/L) | c1 | c2 | |
| C的体积分数 | w1 | w3 | |
| 混合气体密度(g/L) | ρ1 | ρ2 |
| A.若x<4,则2c1<c2 |
| B.若w3=w1,可断定x=4 |
| C.无论x的值是多少,均有2ρ1=ρ2 |
| D.容器甲中反应从开始到达平衡平均速率为v(A)=0.3mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加压有利于SO2与O2反应生成SO3 |
| B.温度过高对合成氨反应不利 |
| C.高温及加入催化剂都能使合成氨的反应速率加快 |
| D.用过量空气煅烧硫铁矿可以提高原料的利用率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小 |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 催化剂 |
| A.更换高效催化剂 | B.增大CO的浓度 |
| C.降低温度 | D.增大压强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
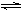 NH3(g) + HI(g) b.2HI(g)
NH3(g) + HI(g) b.2HI(g) 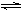 H2(g) + I2(g)
H2(g) + I2(g)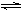 2NH3(g) ΔH=-92.60 kJ·mol-1
2NH3(g) ΔH=-92.60 kJ·mol-1| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | | 1.00 | 1.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com