
ij��Һ�п��ܺ�������6�������е�ij����:Cl-��S��C��N��Na+��K+��Ϊȷ����Һ��ɽ�������ʵ��:
(1)200 mL������Һ,��������BaCl2��Һ,��Ӧ�������ˡ�ϴ�ӡ�����,�ó���4.30 g,������м������������,��2.33 g�������ܡ�
(2)��(1)����Һ�м���������NaOH��Һ,����,������ʹʪ���ɫʯ����ֽ����������1.12 L(�ѻ���ɱ�״��,�ٶ��������� ��ȫ���ݳ�)��
��ȫ���ݳ�)��
�ɴ˿��Եó�����ԭ��Һ��ɵ���ȷ������(��)
A.һ������S��C��N,���ܴ���Cl-��Na+��K+
B.һ������S��C��N��Cl-,һ��������Na+��K+
C.c(C)=0.01 mol��L-1,c(N)>c(S)
D.�������6�����Ӷ�����,��c(Cl-)>c(S)
D������:n(BaSO4)==0.01 mol;n(BaCO3) ==0.01 mol;n(NH3)==0.05 mol;���ݵ������Һ�����ӵ���غ��ϵ:n(N)+n(Na+)+n(K+)=n(Cl-)+2n(C)+2n(S),0.05 mol+n(Na+)+n(K+)=n(Cl-)+2��0.01 mol+2��0.01 mol,n(Cl-)=n(Na+)+n(K+)+0.01 mol>0.01 mol,��n(Cl-)һ������,Na+��K+���ܴ���,A��B�����ȷ;c(C)=0.01 mol��0.2 L=0.05 mol��L-1,C���ȷ;c(Cl-)>0.01 mol,n(S)=0.01 mol,��c(Cl-)>c(S),D����ȷ��
==0.01 mol;n(NH3)==0.05 mol;���ݵ������Һ�����ӵ���غ��ϵ:n(N)+n(Na+)+n(K+)=n(Cl-)+2n(C)+2n(S),0.05 mol+n(Na+)+n(K+)=n(Cl-)+2��0.01 mol+2��0.01 mol,n(Cl-)=n(Na+)+n(K+)+0.01 mol>0.01 mol,��n(Cl-)һ������,Na+��K+���ܴ���,A��B�����ȷ;c(C)=0.01 mol��0.2 L=0.05 mol��L-1,C���ȷ;c(Cl-)>0.01 mol,n(S)=0.01 mol,��c(Cl-)>c(S),D����ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�л������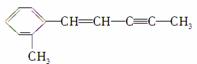 ������ж��ٸ�ԭ�ӹ���(����)
������ж��ٸ�ԭ�ӹ���(����)
A��12��������B��16��������C��20��������D��24
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ǧ���仯������������ء������豸��X���߷������ϵȡ��ش��������⣺
��1��Ǧ��̼��ͬ��Ԫ�أ���̼��4�����Ӳ㣬Ǧ��Ԫ�����ڱ���λ��Ϊ ������������ˮ���������Pb��C�� ���ǿ������������
��2��PbO2��Ũ���Ṳ�����ɻ���ɫ���壬��Ӧ�Ļ�ѧ����ʽΪ ��
��3��PbO2����PbO�����������Һ��Ӧ�Ƶ÷�Ӧ�����ӷ���ʽΪ ��
PbO2Ҳ����ͨ��ʯīΪ�缫Pb(NO3)2��Cu(NO3)2�Ļ����ҺΪ���Һ�����ȡ�����������ĵ缫��ӦʽΪ_ _�������Һ�в�����Cu(NO3)2����Ҫȱ���� ��
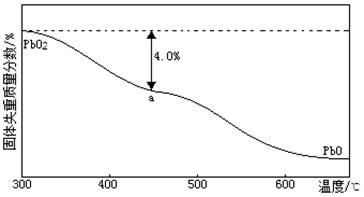
��4��PbO2�ڼ��ȹ��̷����ֽ��ʧ����������ͼ��ʾ����֪ʧ�������ϵ�a��Ϊ��Ʒʧ��4.0%�� ���IJ������壬��a�������ɱ�ʾΪPbOX��mPbO2·nPbO����ʽ����xֵ��m:nֵ_ ��
���IJ������壬��a�������ɱ�ʾΪPbOX��mPbO2·nPbO����ʽ����xֵ��m:nֵ_ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͬ�������ͬpH��ijһԪǿ����Һ�ٺ�ijһԪ������Һ�ڷֱ���������п�۷�����Ӧ�����й����������(V)��ʱ��(t)�仯��ʾ��ͼ��ȷ����(����)
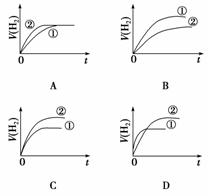
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪:H2O(g) H2O(l)����H1=-Q1 kJ��mol-1(Q1>0)
H2O(l)����H1=-Q1 kJ��mol-1(Q1>0)
C2H5OH(g) C2H5OH(l)����H2=-Q2 kJ��mol-1(Q2>0)
C2H5OH(l)����H2=-Q2 kJ��mol-1(Q2>0)
C2H5OH(g)+3O2(g) 2CO2(g)+3H2O(g)����H3=-Q3 kJ��mol-1(Q3>0)
2CO2(g)+3H2O(g)����H3=-Q3 kJ��mol-1(Q3>0)
��ʹ23 gҺ̬�Ҵ���ȫȼ��,���ָ�����,��ų�������Ϊ(��λΪkJ)(��)
A.Q1+Q2+Q3
B.1.5Q1-0.5Q2+0.5Q3
C.0.5(Q1+Q2+Q3)
D.0.5Q1-1.5Q2+0.5Q3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
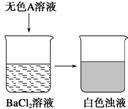
�ճ������е����������뻯ѧ��Ӧ�йأ�����������������ԭ��Ӧ�ص���(����)
A��ͭ�������ϳ���ͭ��[Cu2(OH)2CO3] B�����Ʋ˵�����
C������ʯ�������긯ʴ�ٻ� D�����������������ܵ�����Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��ӦCl2��H2O===HCl��HClO���Ը÷�Ӧ��˵����ȷ����(����)
A��Cl2����������H2O�ǻ�ԭ�� B���������뻹ԭ�������ʵ���֮����1��2
C�����ջ�ѧ����ʽ���У�������ʧ����1 mol D��Cl2�������������ǻ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���г���(������Ϊ����)��ѡ�õ��Լ���������������ȷ��һ����(����)
| ѡ�� | ���ᴿ������ | ѡ�õ��Լ� | �������� |
| A | NaOH(Na2CO3) | ���� | �� |
| B | CO2(CO) | CuO | ���� |
| C | Fe(Zn) | ϡ���� | ���� |
| D | CO2(HCl) | Na2CO3��Һ | ϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ȼ�ԭ��ұ�������ķ�Ӧһ����
(����)��
A���û���Ӧ B���ֽⷴӦ
C�����ֽⷴӦ D��������ԭ��Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com