
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水,乙醇 | 可溶于水,乙醇,三氯乙醛 | 微溶于水,可溶于乙醇 |
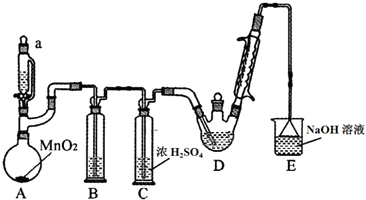
分析 A装置利用二氧化锰与浓盐酸制备氯气,反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,B装置用饱和食盐水除去HCl,C装置盛放浓硫酸干燥氯气,D中反应制备CCl3CHO,E装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl防止污染空气.
(1)由仪器的结构,可知仪器a为恒压分液漏斗;冷凝管水流遵循逆流原理,这样冷凝更充分,效果更好;
(2)浓盐酸易挥发,制得的氯气中含有氯化氢,用饱和食盐水除去HCl;撤去B装置,增大副反应C2H5OH+HCl→C2H5Cl+H2O的发生;
(3)有机物易挥发性,冷凝回流挥发的有机物;E装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl,氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,HCl与氢氧化钠反应生成氯化钠与水;
(4)根据CCl3COOH溶于乙醇与CCl3CHO分析;
(5)根据消耗的Na2S2O3计算剩余I2的物质的量,进而计算与HCOO-反应的I2的物质的量,再根据关系式:CCl3CHO~HCOO-~I2计算;
(6)A.酸性越强,电离程度越大,溶液pH越小;
B.电离程度越大,酸性越强,溶液中离子浓度越大,导电能力越强;
C.酸性越弱,其钠盐的水解程度越大,溶液pH越大.
解答 解:(1)由仪器a的结构可知,该分液漏斗能平衡压强,使漏斗内液体顺利滴下,为恒压分液漏斗,冷凝管水流遵循逆流原理,水流方向是下口进上口出,
故答案为:恒压分液漏斗;下口进上口出;
(2)浓盐酸制取的氯气中含有氯化氢和水蒸气杂质,应用饱和的食盐水除掉氯化氢,当含氯化氢的氯气通过饱和食盐水时,氯化氢溶解在其中,氯气几乎不溶,氯气能与水反应生成HCl与HClO,会发生:CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl、C2H5OH+HCl→C2H5Cl+H2O,导致装置D中副产物:CCl3COOH、C2H5Cl增多,
故答案为:饱和食盐水;CCl3COOH、C2H5Cl;
(3)E装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl防止污染空气,反应离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O; H++OH-=H2O;
(4)CCl3COOH溶于乙醇与CCl3CHO,应采取蒸馏方法进行分离,
故答案为:不可行,三氯乙酸可溶于乙醇、三氯乙醛;
(5)根据消耗的Na2S2O3计算
剩余I2的物质的量0.02000mol•L-1×0.02L×$\frac{1}{2}$=2×10-4mol,与HCOO-反应的I2的物质的量为0.1000mol•L-1×0.02L-2×10-4mol=1.8×10-3mol,由CCl3CHO~HCOO-~I2可知,CCl3CHO的物质的量为1.8×10-3mol,则产品的纯度为$\frac{1.8×1{0}^{-3}mol×147.5g/mol}{0.4g}$×100%=66.4%,
故答案为:66.4%;
(6)A.分别测定0.1mol•L-1两种酸溶液的pH,三氯乙酸的pH较小,说明三氯乙酸电离程度比乙酸的大,则三氯乙酸的酸性比乙酸的强,故A正确;
B.用仪器测量浓度均为0.1mol•L-1的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱,三氯乙酸溶液中离子浓度更大,说明三氯乙酸电离程度比乙酸的大,则三氯乙酸的酸性比乙酸的强,故B正确;
C.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH较大,说明乙酸钠的水解程度更大,则乙酸的酸性比三氯乙酸的弱,故C正确;
故答案为:ABC.
点评 本题考查三氯乙醛的制备,关键是明确反应原理与各装置作用,掌握常用物质分离提纯方法,注意对题目信息的应用,题目难度中等.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 溶有1molFe(OH)3的胶体中,含有NA个Fe(OH)3胶粒 | |
| B. | 在标准状况下,22.4L水的分子数为NA | |
| C. | 常温常压下,14 gC2H4和 C3H6 的混合物含有的氢原子数为2NA | |
| D. | 1molFe与足量Cl2反应,铁失去电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
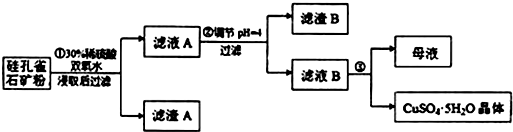
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 完全沉淀的pH | 5.2 | 3.7 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁在潮湿空气中生锈是自发过程 | B. | 有些放热反应常温下是非自发的 | ||
| C. | 自发反应都是熵增大的反应 | D. | 电解池的反应不都是非自发反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使蒸发皿中的水分完全蒸干后,才能停止加热 | |
| B. | 加入盐酸,放出无色无味气体,该气体能使澄清石灰水变浑浊的气体,则原溶液中只含CO32- | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 除去铜粉中混有的少量镁粉和铝粉可加入足量氢氧化钠溶液,反应后过滤、洗涤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com