
����Ŀ�����÷��෨�о���ѧ���ʿ�ϵͳ��ȫ����ʶ���ʵ����ʡ�
I�������������У�����һ�����ʵ�������������ֲ�ͬ��
��MgO��![]() ��
��![]() ��CuO
��CuO
��HCl��![]() ��
��![]() ��
��![]()
��NaOH��![]() ��KOH��
��KOH��![]()
��1����������������![]() �ѧʽ
�ѧʽ![]() ��
��
��______����______����______��
��2����������������ÿ�����һ��������![]() ���÷�Ӧ______
���÷�Ӧ______![]() ������������������
������������������![]() ������ԭ��Ӧ��
������ԭ��Ӧ��
��3��д��![]() ������ϡ���ᷴӦ�����ӷ���ʽ��______��
������ϡ���ᷴӦ�����ӷ���ʽ��______��
��4��![]() ��
��![]() ��
��![]() ����Һ�����ܴ������棬�������ӷ���ʽ˵����____________________________��________________________________________________
����Һ�����ܴ������棬�������ӷ���ʽ˵����____________________________��________________________________________________
���𰸡�CO2 H2O Na2CO3 ���� CO32+2H+�TH2O+CO2�� HCO3+H+=CO2��+H2O HCO3+OH=CO32+H2O
��������
��1������CO2�Ƿǽ���������������ǽ������������H2O�����ᣬ�������������Na2CO3���Σ��������Ǽ
��2����Ӧ��Ԫ��û�м�̬�仯�IJ���������ԭ��Ӧ��
��3��Na2CO3�ǿ������Σ�������ǿ�ᣬ���ӷ�Ӧ���ܲ�Na2CO3������ϡ���ᷴӦ���ɶ�����̼��ˮ�������ƣ�
��4��HCO3-���������ʽ������ӣ�����H+��OH-��Ӧ��
��1������CO2�Ƿǽ���������������ǽ������������H2O�����ᣬ�������������Na2CO3���Σ��������Ǽ
�ʴ�Ϊ��CO2��H2O��Na2CO3��
��2����ѧ��ӦΪ��Na2CO3+CO2+H2O�T2NaHCO3����Ӧ��Ԫ��û�м�̬�仯������������ԭ��Ӧ��
�ʴ�Ϊ�����ǣ�
��3��Na2CO3������ϡ���ᷴӦ���ɶ�����̼��ˮ�������ƣ�Na2CO3��Na2SO4�ǿ������Σ�������ǿ�ᣬ���ӷ�Ӧ�о��ܲ�����Na2CO3������ϡ���ᷴӦ�����ӷ���ʽΪ��CO32+2H+�TH2O+CO2����
�ʴ�Ϊ��CO32+2H+�TH2O+CO2����
��4��HCO3���������ʽ������ӣ�����H+��OH��Ӧ�������ӷ���ʽ�ֱ�Ϊ��HCO3+H+=CO2��+H2O��HCO3+OH=CO32+H2O��
�ʴ�Ϊ��HCO3+H+=CO2��+H2O��HCO3+OH=CO32+H2O��


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѹǿΪ0.1MPa�����£��ݻ�ΪV L���ܱ�������a mol CO��2a mol H2�ڴ��������·�Ӧ���ɼ״���CO��g��+2H2��g��![]() CH3OH��g����CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ����
CH3OH��g����CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ����
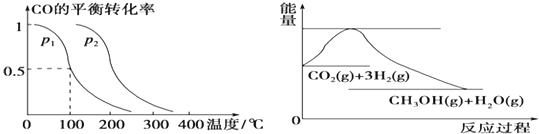
��1����p1________p2����������������������=������
���������������������£���������������a mol CO��2a mol H2���ﵽ��ƽ��ʱ��CO��ƽ��ת����________������������������С����������������
����p1�£�100��ʱ��CO��g��+2H2��g��![]() CH3OH��g����Ӧ��ƽ�ⳣ��Ϊ______���ú�a��V�Ĵ���ʽ��ʾ����
CH3OH��g����Ӧ��ƽ�ⳣ��Ϊ______���ú�a��V�Ĵ���ʽ��ʾ����
��2����ͼ��ʾCO2��H2��Ӧ����CH3OH��H2O�Ĺ�������������λΪkJmol��1���ı仯���÷�Ӧ�ġ�H_________0����S_______0��
��3��Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1L���ܱ������У�����1mol CO2��3mol H2�� һ�������·�����Ӧ��CO2��g��+3H2��g��![]() CH3OH��g��+H2O��g�������CO2��g����CH3OH��g����Ũ����ʱ��仯��������ͼ��ʾ��
CH3OH��g��+H2O��g�������CO2��g����CH3OH��g����Ũ����ʱ��仯��������ͼ��ʾ��
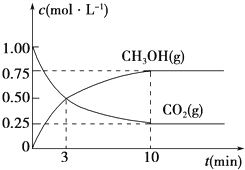
�ٴӷ�Ӧ��ʼ��ƽ�⣬CO2��ƽ����Ӧ����v��CO2��=_________________________��
�����д�ʩ����ʹ��ѧƽ��������Ӧ�����ƶ�����________�����ţ���
A�������¶�
B����CH3OH��g����ʱҺ���Ƴ�
C��ѡ���Ч����
D���ٳ���1mol CH3OH��g����1mol H2O��g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п���仯������;�㷺������п����п����Ҫ�ɷ���ZnS��Ϊ��Ҫԭ�ϣ��漰����Ҫ��Ӧ�У���2ZnS��s��+3O2��g��=2ZnO��s��+2SO2��g����H1=��930kJmol-1
��2C��s��+O2��g��=2CO��g����H2=��221kJmol-1
��ZnO��s��+CO��g��=Zn��g��+CO2��g����H3=+198kJmol-1
��1����ӦZnS��s��+C��s��+2O2��g��=Zn��g��+CO2��g��+SO2��g���ġ�H4=____kJmol-1��
��Ӧ�����ɵ�CO2��NH3��ϣ���һ�������·�Ӧ�ϳ����أ�2NH3��g��+CO2��g��![]() CO��NH2��2��s��+H2O��g�� ��H�����÷�Ӧ��һ���¡������ܱ������ڽ��У��жϷ�Ӧ�ﵽƽ��״̬�ı�־��___��
CO��NH2��2��s��+H2O��g�� ��H�����÷�Ӧ��һ���¡������ܱ������ڽ��У��жϷ�Ӧ�ﵽƽ��״̬�ı�־��___��
a��CO2��H2O��g��Ũ����� b�������������ѹǿ���ٸı�
c��2v��NH3����=v��H2O���� d�������л��������ܶȲ��ٸı�
��2����������(NOCl)���л��ϳ��е���Ҫ�Լ�������NO��Cl2��һ�������ºϳɣ�2NO(g)+Cl2(g)![]() 2NOCl(g) ��H��0�����ֺ��º��������������ʵ���֮��Ϊ3mol��NO��Cl2�Բ�ͬ�ĵ��ȱ�[n(NO)/n(Cl2)]���з�Ӧ��ƽ��ʱij��Ӧ���ת�����뵪�ȱȼ���ͬ�¶ȵĹ�ϵ��ͼ��ʾ��
2NOCl(g) ��H��0�����ֺ��º��������������ʵ���֮��Ϊ3mol��NO��Cl2�Բ�ͬ�ĵ��ȱ�[n(NO)/n(Cl2)]���з�Ӧ��ƽ��ʱij��Ӧ���ת�����뵪�ȱȼ���ͬ�¶ȵĹ�ϵ��ͼ��ʾ��
��ͼ��T1��T2�Ĺ�ϵΪ��T1___T2(���������������=��)��
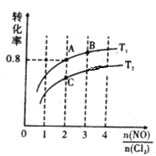
��ͼ��������Ϊ����___��ת���ʣ�
��ͼ��A��B��C�����Ӧ��NOCl�������������____(�A������B������C��)��
���������ݻ�Ϊ2L����B���ƽ�ⳣ����ֵΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������ԭ��Ӧ���ǣ�������
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ڣ�100 ���ĵ����ºϳ�һ����X���˷��ӵ�ģ������ͼ(ͼ�е����߱�ʾ��ѧ��)������˵����ȷ���ǣ� ��
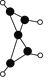
A. X��ʹ������Ȼ�̼��Һ��ɫ
B. X��һ���ڳ��������ȶ����ڵ�Һ̬��
C. X��������ͬһƽ���ϵ�̼ԭ�������5��
D. ���ȼ�յ�������X�ͼ��飬X����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����
ʵ������ȡ��ϩ�����Ҵ���Ũ���ᷴӦ�������¶ȹ��߶���������Ӧ����̿�ڡ�������������̼��ˮ������������ͼ���Ϊ��~��ʵ��װ�ã����һ��ʵ�飬����֤������Ӧ��Ļ�������к��ж�����������̼��ˮ������

��1����װ�õı�ű�ʾ������˳�������������ҵ�����6������ ������3������ ������ ������ ��____
��2��װ�â��еĹ���ҩƷΪ____��������֤�IJ�����____��
��3��װ�â��е���Һ��____��������֤�IJ�����____��
��4��װ�â��е�Ʒ����Һ������_____��
��5��װ�â�����ˮ��������____��д�����п��ܷ�����2����ѧ����ʽ____��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������װ��(��)�����÷�����������������һ����ԭ�ӻ��˸��ǻ��γɣ�����˵������ȷ����
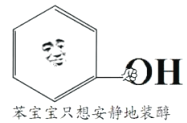
A. ������ֻ�밲����װ����˵���÷��Ӳ��Ǵ�
B. �÷���������ԭ��һ������
C. �÷����ܺ�Na�����û���Ӧ����H2
D. �÷��ӱ����ϵ�һ����ԭ�ӱ���C4H9ȡ�����õ�ͬ���칹����12��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����I2(g)��H2(g)![]() 2HI(g)��26.5kJ����I2(s)��H2(g)
2HI(g)��26.5kJ����I2(s)��H2(g)![]() 2HI(g)��9.5kJ�����з�����ȷ����
2HI(g)��9.5kJ�����з�����ȷ����
A.���Ƿ��ȷ�Ӧ��������ȼ��ɷ���
B.����������ϼ��Ȳ��ܷ�����Ӧ
C.I2(g)��I2(s)��������ϵ��ͼ��ʾ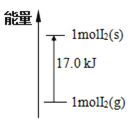
D.1molI2(s)��1molH2(g)������֮�ͱ�2molHI(g)������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ksp��AgCl��=1.56��10��10��Ksp��AgBr��=7.7��10��13 ��Ksp��Ag2CrO4��=9��10��11��ij��Һ�к���Cl����Br����CrO42����Ũ�Ⱦ�Ϊ0.010mol/L�������Һ����μ���0.010mol/L��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ( )
A. Cl����Br����CrO42��B. Br����Cl����CrO42��
C. CrO42����Br����Cl��D. Br����CrO42����Cl��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com