
一定条件下,在恒容密闭容器中,能表示反应X(g)+2Y(g)  2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.①④
C.②③ D.③④
科目:高中化学 来源: 题型:
有下列化学仪器:
①托盘天平 ②玻璃棒 ③药匙 ④烧杯 ⑤量筒 ⑥容量瓶 ⑦胶头滴管 ⑧细口试剂瓶 ⑨标签纸
(1)现需要配制500 mL 1 mol·L-1 H2SO4溶液,需要质量分数为98%、密度为1.84 g·cm-3的浓H2SO4________ mL。
(2)上述仪器中,按实验要求使用的先后顺序,其编号排列是____________________。
(3)容量瓶使用前检验是否漏水的方法是____________________________
__________________________________________________________。
(4)若实验过程中遇到下列情况,对硫酸的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)。
①用来稀释浓硫酸的烧杯未洗涤,________;
②未经冷却将溶液注入容量瓶中,________;
③摇匀后发现液面下降再加水,________;
④定容时俯视观察液面,________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作正确的是
A.用托盘天平称量4.00g氢氧化钠固体 B.用10mL量筒量取8.5mL蒸馏水
C.用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应
D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是

A.原溶液中一定含有SO42-离子 B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:可逆反应2SO2(g)+O2(g)  2SO3(g) ΔH<0,在一定条件下达到平衡后,改变下列条件一定能使该平衡向正反应方向移动的是( )
2SO3(g) ΔH<0,在一定条件下达到平衡后,改变下列条件一定能使该平衡向正反应方向移动的是( )
A.升温增压 B.降温增压
C.升温减压 D.降温减压
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积不变的密闭容器中存在如下反应:2A(g)+B(g)  3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

A.图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响
B.图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
D.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化硫和氮的氧化物是大气的主要污染物,防止和治理其对环境的污染是当前环保工作的重要研究内容之 一。
一。
(1)一定条件下,发生反应2SO2(g)+O2(g)  2SO3(g),向2 L密闭容器中通入2 mol SO2(g)、1 mol O2(g)和0.2 mol SO3(g),2 min后反应达到平衡时,测得SO2的物质的量为1 mol,若往容器中再加入2 mol SO2(g),则重新达到平衡时SO2的总转化率________50%(填“>”、“<”或“=”)。
2SO3(g),向2 L密闭容器中通入2 mol SO2(g)、1 mol O2(g)和0.2 mol SO3(g),2 min后反应达到平衡时,测得SO2的物质的量为1 mol,若往容器中再加入2 mol SO2(g),则重新达到平衡时SO2的总转化率________50%(填“>”、“<”或“=”)。
(2)在一密闭容器中发生反应 2 NO2 2NO+O2
2NO+O2
ΔH>0,反应过程中NO2的浓度随时间变化的情况如下图所示。
请回答: ①依曲线A,反应在前3 min内氧气的平均反
①依曲线A,反应在前3 min内氧气的平均反 应速率为________。
应速率为________。
②若曲线A、B分别表示的是该反应在某不同条件下的反应情况,则此条件可能是____ ____(填“浓度”、“压强”、“温度”或“催化剂”)。
____(填“浓度”、“压强”、“温度”或“催化剂”)。
(3)一定温度下,在密闭容器中N2O5可发生下列反应:
①2N2O5(g)  4NO2(g)+O2(g)
4NO2(g)+O2(g)
②2NO2(g)  2NO(g)+O2(g)
2NO(g)+O2(g)
若达平衡时,c(NO2)=0.4 mol/L,c(O2)=1.3 mol/L,则反应②中NO2的转化率为________,N2O5(g)的起始浓度应不低于________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式表达正确的是
A.用惰性电极电解熔融氯化钠:
2Cl-+2H2O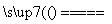 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.用氢氧化钠溶液除去铝表面的氧化膜:
Al2O3+2OH-===2AlO +H2O
+H2O
C.用稀氢氧化钠溶液吸收二氧化氮:
2OH-+2NO2===NO +NO↑+H2O
+NO↑+H2O
D.用食醋除去水瓶中的水垢:
CO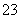 +2CH3COOH===2CH3COO-+CO2↑+H2O
+2CH3COOH===2CH3COO-+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
H2和CO2在高温下发生反应:
CO2(g)+H 2(g)
2(g)  CO(g)+H2O(g)。下表是986℃时,在容积不变的密闭容器中进行反应的四组数据:
CO(g)+H2O(g)。下表是986℃时,在容积不变的密闭容器中进行反应的四组数据:
| 编号 | 起始浓度/mol/L | 平衡浓度/mol/L | ||||||
| c0(H2) | c0(CO2) | c0(H2O) | c0(CO) | c(H2) | c(CO2) | c(H2O) | c(CO) | |
| 1 | 1.0 | 1.0 | 0 | 0 | 0.44 | 0.44 | 0.56 | 0.56 |
| 2 | 1.0 | 2.0 | 0 | 0 | 0.27 | 1.27 | 0.73 | 0.73 |
| 3 | 0 | 0 | 2.0 | 2.0 | 0.88 | 0.88 | 1.12 | 1.12 |
| 4 | 0.2 | 0.4 | 0.6 | 0.8 | 0.344 | 0.544 | 0.456 | 0.656 |
下列叙述中正确的是( )
①该温度下反应的平衡常数约为1.62
②该反应的平衡常数与反应的起始浓度无关
③增大CO2的起始浓度,可使CO2的转化率增大
④从反应开始至达到平衡状态,混合气体的密度没有发生改变
A.②③ B.①②③
C.①②④  D.①③
D.①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com