
| A. | 正极反应式为O2+4e-═2O2- | |
| B. | 放电时溶液中的阳离子向正极方向移动 | |
| C. | 该电池反应为CH4+2O2═CO2+2H2O | |
| D. | 通入CH4一极的电极反应式为CH4+2O2+8e-═CO2+2H2O |
分析 燃料电池中,燃料甲烷在负极失电子被氧化,电极方程式为CH4+10OH--8e-=CO32-+7H2O,通入氧气的一极为原电池的正极,发生还原反应,电极方程式为02+2H2O+4e-=40H-,总反应式为CH4+2O2+2NaOH═Na2CO3+3H2O,以此解答该题.
解答 解:A.通入氧气的一极为原电池的正极,发生还原反应,电极方程式为02+2H2O+4e-=40H-,故A错误;
B.原电池工作时,阳离子向正极移动,故B正确;
C.电解质参加了电池反应,总反应式为CH4+2O2+2NaOH═Na2CO3+3H2O,故C错误;
D.通入甲烷的一极为负极,发生氧化反应,甲烷失去电子,电解质参加反应,电极方程式为CH4+10OH--8e-=CO32-+7H2O,故D错误;
故选:B.
点评 本题考查碱性甲烷燃料电池的工作原理,题目难度中等,本题中注意把握电极反应式的书写,不要忽略电解质溶液参加反应,在学习中注意积累转移电子与参加反应的物质的量的关系.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,1L0.1mol/LNH4NO3溶液中的氮原子数为0.2NA | |
| B. | 常温下,向含1molH2SO4的浓硫酸加入足量的铁粉,转移的电子数为2NA | |
| C. | 标准状况下,2.24L己烷分子中含有1.9NA对共用电子 | |
| D. | 将1mol明矾晶体完全溶于水制成胶体,其中所含胶体微粒数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜锌原电池中铜是负极 | |
| B. | 用电解法精炼粗铜时,纯铜作阳极 | |
| C. | 在镀件上电镀铜时可用金属铜作阳极 | |
| D. | 电解稀硫酸制H2、O2时,铜作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
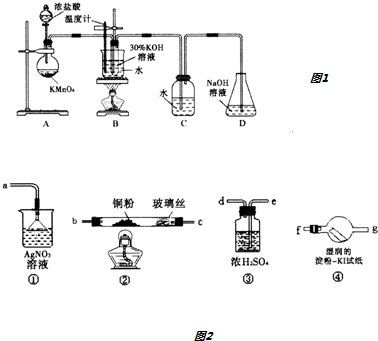
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/ml | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和甲醇 | B. | 丙醛和丙酮 | C. | 乙烯和乙炔 | D. | 乙烯和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18.75% | B. | 30% | C. | 15% | D. | 22.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该 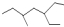 有机物的系统命名为:3-乙基-5-甲基庚烷 有机物的系统命名为:3-乙基-5-甲基庚烷 | |
| B. | 棉花、羊毛、合成纤维、油脂的成分都是高分子化合物 | |
| C. | 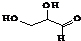 该有机物属于单糖,在一定条件下能发生取代、消去、加成、氧化、还原等反应 该有机物属于单糖,在一定条件下能发生取代、消去、加成、氧化、还原等反应 | |
| D. | 等质量的乙烯和乙醇完全燃烧消耗氧气的量相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com