
科目:高中化学 来源: 题型:阅读理解
| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| b-a-4c |
| 2 |
| b-a-4c |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| c(CH3OH) |
| c(CO)?c(H2)2 |
| c(CH3OH) |
| c(CO)?c(H2)2 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省南安一中高二上学期期末考试化学试卷(带解析) 题型:填空题
(16分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g)  CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1)下列各项中,不能够说明该反应已达到平衡的是__________(填序号)。
A. 恒温、恒容条件下,容器内的压强不发生变化
B. 一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
C. 一定条件下,CO、H2和CH3OH的浓度保持不变
D. 一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
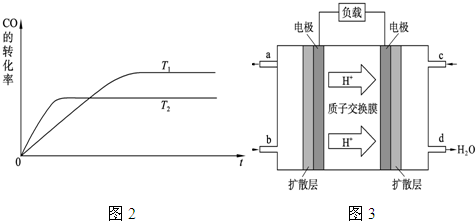
(2) 右图是该反应在不同温度下CO的转化率随时间变化的曲线。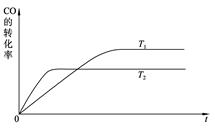
① 该反应的焓变ΔH__________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1_______K2
(填 “>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是
______________。
A. 升高温度 B. 将CH3OH(g)从体系中分离
C. 使用合适的催化剂
D. 充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,甲醇燃料电池的工作原理如右图所示。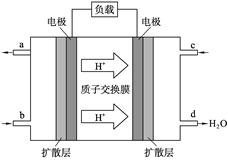
①请写出c口通入的物质发生的相应电极反应式_________ 。
②工作一段时间后,当0.2 mol甲醇完全反应生成CO2 时,有___________NA个电子转移。
(4)利用右装置,可以模拟铁的电化学防护。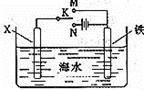
若X为碳棒,为减缓铁的腐蚀,开关K应该置于 处。
若X为锌,开光K置于 处,该电化学防护法称为 。
查看答案和解析>>
科目:高中化学 来源:2014届福建省高二上学期期末考试化学试卷(解析版) 题型:填空题
(16分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g) 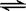 CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1)下列各项中,不能够说明该反应已达到平衡的是__________(填序号)。
A. 恒温、恒容条件下,容器内的压强不发生变化
B. 一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
C. 一定条件下,CO、H2和CH3OH的浓度保持不变
D. 一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2) 右图是该反应在不同温度下CO的转化率随时间变化的曲线。
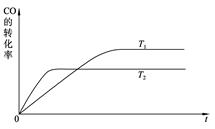
① 该反应的焓变ΔH__________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1_______K2
(填 “>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是
______________。
A. 升高温度 B. 将CH3OH(g)从体系中分离
C. 使用合适的催化剂
D. 充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,甲醇燃料电池的工作原理如右图所示。
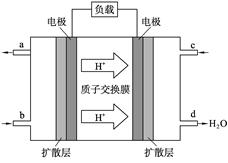
①请写出c口通入的物质发生的相应电极反应式_________ 。
②工作一段时间后,当0.2 mol甲醇完全反应生成CO2 时,有___________NA个电子转移。
(4)利用右装置,可以模拟铁的电化学防护。
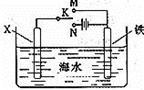
若X为碳棒,为减缓铁的腐蚀,开关K应该置于 处。
若X为锌,开光K置于 处,该电化学防护法称为 。
查看答案和解析>>
科目:高中化学 来源:2014届吉林省高二上学期期末考试化学试卷(解析版) 题型:填空题
(18分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)? ?CH3OH(g)。
?CH3OH(g)。
(1)分析该反应并回答下列问题:
①平衡常数表达式为K=__________________。
②下列各项中,不能够说明该反应已达到平衡的是________(填序号)。
A、恒温、恒容条件下,容器内的压强不发生变化
B、一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
C、一定条件下,CO、H2和CH3OH的浓度保持不变
D、一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2)下图是该反应在不同温度下CO的转化率随时间变化的曲线。

①该反应的焓变ΔH________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是________。
A、升高温度
B、将CH3OH(g)从体系中分离
C、使用合适的催化剂
D、充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。

①该电池工作时,b口通入的物质为______________,c口通入的物质为_____________。
②该电池正极的电极反应式为:________。
③工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有_____________NA个电子转移。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com