
已知X的最高价氧化物对应的水化物化学式为H2XO3,Y是地壳中含量最高的元素,则XY2由固态变为气态所需克服的微粒间作用力是________;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称______。
★ ★★
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
铁是最常见的金属之一,铁可以形成多种氧化物、氢氧化物和盐类。铁与二氧化碳、水在某一密闭体系中反应情况如下表所示:
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1 173K | ||
| ①Fe(s)+CO2(g)FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)CO2(g)+H2(g) | K3 | ? | ? |
完成下列填空:
(1)反应①为______(填“吸热”或“放热”)反应。根据反应①与②可以推导出同温下K1、K2与K3之间的关系,则K3=______(用K1、K2表示)。
(2)973 K时,若反应③在一个容积为2 L的反应容器内2 min时达到平衡,有3 mol电子发生转移,则在2 min内v(CO2)=____________。若压缩容器的容积为原来的一半,平衡将______移动(填“向左”、“向右”或“不”),CO2的浓度将______(填“增大”、“减小”或“不变”)。使该反应的平衡转化率及平衡常数都增大的措施有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中的两种固态物质熔化(或升华)时,克服的微粒间相互作用力属于同种类型的是( )
A.碘和碘化钠
B.金刚石和重晶石
C.冰醋酸和硬脂酸甘油酯
D.干冰和二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.在分子中,两个成键的原子间的距离叫做键长
B.H—Cl的键能为431.8 kJ·mol-1,H—I的键能为298.7 kJ·mol-1,这可以说明HCl分子比HI分子稳定
C.含有极性键的分子一定是极性分子
D.键能越大,表示该分子越容易受热分解
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中不存在氢键的是 ( )
A.液态甲烷中甲烷分子之间
B.液态氟化氢中氟化氢分子之间
C.一水合氨分子中的氨分子与水分子之间
D.可燃冰(CH4·8H2O)中甲烷分子与水分子之间
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
答案 (1)1∶3
(2)①2NO2+2NaOH===NaNO3+NaNO2+H2O
②NaNO2
(3)①Na2CO3+2NO2===NaNO3+NaNO2+CO2
②NaNO3:0.05 mol NaNO2:0.15 mol 0.5
解析 (1)设NO的体积为V(NO),NO2的体积为V(NO2),依据方程式知,处理NO需NH3: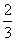 V(NO),处理NO2需NH3:
V(NO),处理NO2需NH3: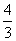 V(NO2),则
V(NO2),则
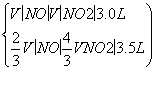
解得V(NO)=0.75 L
V(NO2)=2.25 L
V(NO)∶V(NO2)=1∶3。
(2)①生成两种钠盐,必然是NO2的歧化反应,依据量的关系可知两种盐分别为NaNO3和NaNO2。
②NO中氮的化合价为+2价,NO2中氮的化合物为+4价,二者1∶1混合时与NaOH反应生成一种钠盐,依据电子守恒可知,钠盐中氮的化合价为+3,即为NaNO2。
(3)②n(NO2)=0.15 mol,n(NO)=0.05 mol
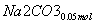 +
+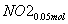 +
+ ===
===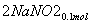 +CO2
+CO2
则单独与Na2CO3反应的NO2为0.15 mol-0.05 mol=0.1 mol
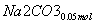 +
+ ===
===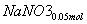 +
+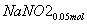 +CO2
+CO2
所以共生成NaNO3:0.05 mol,NaNO2:0.15 mol
c(Na2CO3)= =0.5 mol·L-1。
=0.5 mol·L-1。
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
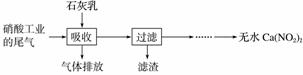
(2)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是________________________;滤渣可循环使用,滤渣的主要成分是________(填化学式)。
(3)该工艺需控制NO和NO2物质的量之比接近1∶1。若n(NO)∶n(NO2)>1∶1,则会导致__________________;若n(NO)∶n(NO2)<1∶1,则会导致________________________________________________________________________。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
在基态多电子原子中,关于核外电子能量的叙述错误的是( )
A.最易失去的电子能量最高 B.电离能最小的电子能量最高
C.p轨道电子能量一定高于s轨道电子能量 D.在离核最近区域内运动的电子能量最低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com