
下列说法错误的是
A.电解饱和食盐水可制取烧碱、氯气、氢气
B.从海水中可提取镁、溴、碘等物质
C.粗铜(含少量Zn、Fe、Pt等)电解精炼后,溶液中金属阳离子只有Fe2+、Zn2+
D.在镀件上镀铜,镀件作阴极
科目:高中化学 来源:2014-2015学年河北省唐山市高三上学期期末理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列叙述中正确的是
A.足量铁在氯气中反应,l mol铁失去的电子数为2 NA
B.标准状况下22.4 L H2中含中子数为2 NA
C.1 L Imol/L的盐酸溶液中,所含氯化氢分子数为NA
D.常温下46 g NO2和N2O4混合气体中含有原子数为3NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
下图所示与对应叙述相符的是
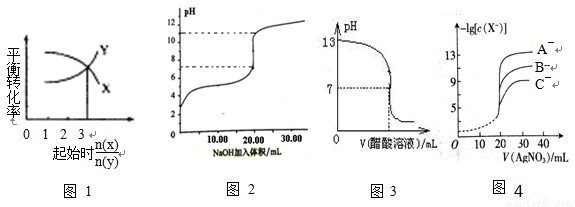
A.一定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X + 3Y Z
Z
B.图2表示NaOH溶液滴加到0.1 mol/L的一元酸溶液得到的滴定曲线(常温下),该实验最好选取酚酞作指示剂
C.常温下,向NaOH溶液中逐滴加入等浓度的醋酸溶液,所得滴定曲线如图3所示。当7<pH<13 时,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图4可确定首先沉淀的是C-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:实验题
(11分)果汁在生产过程中添加亚硫酸及其盐类,以抑制有害微生物的生长及抗氧化。某化学兴趣小组查阅文献后,用下图所示装置测定某果汁样品中SO2残留量。
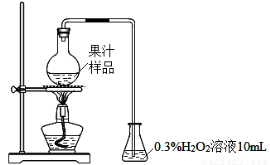
实验步骤:
(ⅰ)在烧瓶中加入50.00 mL果汁样品与3mL浓硫酸的混合液,加热10 min。
(ⅱ)移出锥形瓶,迅速滴入2~3滴酚酞试液,用0.01000 mol·L-1NaOH标准溶液滴定。
回答问题:
(1)实验室配制NaOH标准溶液时,不需要用到的仪器是 。
A.容量瓶 B.胶头滴管 C.烧瓶 D.玻璃棒
(2)将50. 00 mL果汁样品与3mL浓硫酸混合的操作是 。
(3)锥形瓶中发生反应的离子方程式是 。
(4)若步骤(ⅱ)消耗NaOH标准溶液25. 00 mL,则果汁样品中SO2残留量是 g/L。
(5)若改用0.5%的碘水10 mL作吸收液,实验中消耗NaOH标准溶液体积 。
A.V = 25 mL B.25 mL<V<50 mL C.V>50 mL
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:选择题
下列各选项所描述的两个量中,前者一定大于后者的是
A.NH4NO3溶液中NH4+和NO3-的数目
B.纯水在80℃和25℃时的pH
C.pH与体积都相同的氨水和NaOH溶液分别用0.1 mol·L-1盐酸恰好中和,所需的盐酸体积
D.相同温度下,pH =12的NaOH溶液和Na2CO3溶液中由水电离出的c (OH-)
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省咸宁市高一上学期期末考试化学(B)试卷(解析版) 题型:填空题
向含2 mol H2SO4和1 mol HNO3的混合稀溶液中加入过量的锌,假设HNO3被还原的产物全部为NO。
①写出反应的离子方程式 。
②生成的气体在标况下的体积为: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省咸宁市高一上学期期末考试化学(B)试卷(解析版) 题型:选择题
根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是
①Cl2+2KI===I2+2KCl ②2FeCl3+2HI===I2+2FeCl2+2HCl
③2FeCl2+Cl2===2FeCl3 ④I2+SO2+2H2O===2HI+H2SO4
A、Cl2>I2>Fe3+>SO2 B、Fe3+>Cl2>I2>SO2
C、Cl2>Fe3+>I2>SO2 D、Cl2>Fe3+>SO2>I2
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省咸宁市高二上学期期末考试化学(B)试卷(解析版) 题型:填空题
(12分)(1)物质的量浓度相同的下列物质的溶液①NH4Cl ②NH4HSO4 ③CH3COONH4,c(NH4+)由小到大的顺序是 (填序号)。
(2)同浓度的下列溶液:①CH3COONH4 ②NH4Cl ③Na2CO3 ④NaHCO3,其中pH由大到小的顺序 是 。
(3)物质的量浓度相同的 ①盐酸、②硫酸溶液、 ③醋酸(CH3COOH)溶液各100 mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、V2、V3,它们由大到小的顺序是 。
(4)CH3COONa溶液呈 性(填“酸”、“碱”或“中”),其原因是 (用离子方程式表示)。
(5)常温时,若10体积pH1=a的盐酸溶液与1体积pH2=b的氢氧化钠溶液混合后溶液呈中性,则混合前该强酸的pH1与强碱的pH2之间应满足的关系是_________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省荆门市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列实验方案的设计中,不可行的是
A.用溶解、过滤的方法分离KNO3和NaCl固体的混合物
B.用萃取的方法分离水和四氯化碳
C.加稀盐酸后过滤,除去混在铜粉中的少量铁粉和铝粉
D.将氧气和氮气的混合气体通过灼热的铜网,以除去其中的氧气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com