
| A. | 氟原子的结构示意图: | B. | 塑料王聚四氟乙烯的结构简式: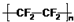 | ||
| C. | 中子数为10的氟原子:${\;}_{9}^{19}$F | D. | 萤石主要成分CaF2电子式: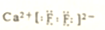 |
分析 A.氟原子的核电荷数为9,最外层含有7个电子;
B.F2C=CF2加聚反应产物为聚四氟乙烯;
C.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
D.氟化钙为离子化合物,钙离子直接用离子符号Ca2+表示,氟离子需要标出其最外层电子及所带电荷,两个氟离子需要先在钙离子的两边.
解答 解:A. 为氟离子结构示意图,氟原子的核电荷数=核外电子总数=9,其正确的原子结构示意图为:
为氟离子结构示意图,氟原子的核电荷数=核外电子总数=9,其正确的原子结构示意图为: ,故A错误;
,故A错误;
B.聚四氟乙烯为四氟乙烯的加聚反应产物,聚四氟乙烯的结构简式为: ,故B正确;
,故B正确;
C.中子数为10的氟原子的质量数为19,其表示方法为:${\;}_{9}^{19}$F,故C正确;
D.氟化钙为离子化合物,钙离子直接用离子符号Ca2+表示,氟离子需要标出其最外层电子及所带电荷,两个氟离子需要先在钙离子的两边,氟化钙的电子式为: ,故D错误;
,故D错误;
故选BC.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及结构简式、原子结构示意图、元素符号、电子式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 稀释前,溶液pH:①>②=③ | |
| B. | 稀释后,溶液pH:①>②=③ | |
| C. | 稀释前,溶液中溶质的物质的量浓度:③>①=② | |
| D. | 稀释后,溶液中溶质的物质的量浓度:③>①=② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 实验室需要0.1mol/L NaOH溶液450mL,需要0.5mol/L硫酸溶液500mL.根据这两种溶液的配置情况回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL,需要0.5mol/L硫酸溶液500mL.根据这两种溶液的配置情况回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
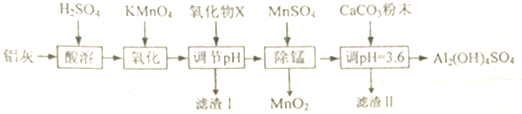
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 常温下,21gC3H6和C4H8的混合物中含有的碳原子数为1.5NA | |
| C. | 46g乙醇中含有C-H键的数目为6NA | |
| D. | 常温下,2.7g金属铝与足量浓度为18mol/L的浓硫酸反应时转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 阴离子的还原性:Y>X | |
| B. | Y和Z的简单阴离子都会破坏水的电离平衡 | |
| C. | 最高价氧化物的水化物的酸性:Z>Y | |
| D. | 氢化物的热稳定性:W>X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com