
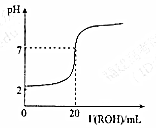
 室温时,往20mL 0.1mol•L-1的HM酸溶液中逐滴滴入0.1mol•L-1的ROH碱溶液,溶液的pH与所加的ROH溶液的体积关系如图所示,下列说法正确的是( )
室温时,往20mL 0.1mol•L-1的HM酸溶液中逐滴滴入0.1mol•L-1的ROH碱溶液,溶液的pH与所加的ROH溶液的体积关系如图所示,下列说法正确的是( )| A. | V(ROH)<20mL时,随着V(ROH)增大,HM的电离程度减小 | |
| B. | K(HM)=K(ROH) | |
| C. | RM不能发生水解反应 | |
| D. | V(ROH)>20mL时,溶液中c(R+)<c(M-) |
分析 0.1mol•L-1的HM酸溶液pH大于2,说明HM为弱酸,逐滴滴入0.1mol•L-1的ROH碱溶液20mL时pH=7,说明溶液呈中性,则ROH为弱碱,且二者电离程度相等,以此解答该题.
解答 解:A.HM为弱酸,加入ROH,发生中和反应,促进电离,故A错误;
B.逐滴滴入0.1mol•L-1的ROH碱溶液20mL时pH=7,说明溶液呈中性,则ROH为弱碱,且二者电离程度相等,则K(HM)=K(ROH),故B正确;
C.MR为弱酸弱碱盐,可发生水解,故C错误;
D.V(ROH)>20mL时,碱过量,溶液呈碱性,由电荷守恒c(Na+)+c(H+)=c(OH-)+c(M-)可知c(R+)>c(M-),故D错误.
故选B.
点评 本题考查了物质反应后的溶液酸碱性判断,为高考常见题型,侧重考查学生的分析能力,注意图象的特征分析应用,盐类水解和电解质溶液中电荷守恒的理解应用是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
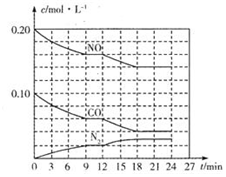 为有效控制雾霾,各地积极采取措施改善大气质量,有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量,有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl溶液呈酸性说明NH3•H2O是弱电解质 | |
| B. | 醋酸钠溶液中c(Na+)>c(CH3COO-) | |
| C. | 常温下相同pH的NaOH溶液和CH3COONa溶液中水电离出的OH-浓度相同 | |
| D. | 常温下,在1mol•L-1的盐酸中加入等体积等浓度的氨水,溶液导电能力减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烟、云、雾在阳光照射下可观察到丁达尔效应 | |
| B. | “温室效应”“酸雨”的形成都与氮氧化合物有关 | |
| C. | 绿色化学的核心是对环境污染进行综合治理 | |
| D. | 高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
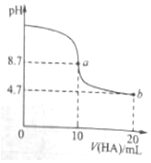 室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10ml 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )| A. | a点所示溶液中c(A-)+c(HA)=0.1mol•L-1 | |
| B. | b点所示溶液中c(HA)>c(A-) | |
| C. | pH=7时,c(Na+)=c(A-)+c(HA) | |
| D. | a、b两点所示溶液中水的电离程度a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2P2(g)=P4(g)△H=-229.7 kJ•mol-1 | B. | P2制P4是放热反应 | ||
| C. | P2比P4更加稳定 | D. | 等质量时P2比P4具有的能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将一定量的NaNO3和KCl混合加热浓缩至有固体析出,过滤. | 有白色晶体析出 | 白色晶体为KNO3 |
| B | 向2mLNaCl和NaI(浓度均为0.1mol•L-1)混合溶液中滴入2滴0.1mol•L-1AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向某溶液中加入盐酸酸化的Ba(NO3)2溶液 | 出现白色沉淀 | 该溶液一定有SO42-或 Ag+ |
| D | 向淀粉水解液中加入新制的Cu(OH)2悬浊液,煮沸 | 没有生成(砖)红色沉淀 | 淀粉未水解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com