
| A. | 氯化钙是中性干燥剂,可用于实验室干燥氨气 | |
| B. | 二氧化氯具有强氧化性,可用于自来水的杀菌消毒 | |
| C. | 常温下,铝与浓硫酸发生钝化,可用铝槽车贮运浓硫酸 | |
| D. | 钠是一种具有强还原性的金属,可用于冶炼钛、锆、铌等金属 |
分析 A.氨气与氯化钙结合生成络合物;
B.二氧化氯具有强氧化性,能够使蛋白质变性;
C.依据浓硫酸的强氧化性解答;
D.钠最外层一个电子,容易失去电子,具有强的还原性.
解答 解:A.氨气与氯化钙结合生成络合物,所以不能用氯化钙干燥氨气,故A错误;
B..二氧化氯具有强氧化性,能够使蛋白质变性,具有杀菌消毒作用,可用于自来水的杀菌消毒,故B正确;
C.常温下,浓硫酸具有强的氧化性,铝与浓硫酸发生钝化,形成致密的氧化膜,阻止反应继续进行,可用铝槽车贮运浓硫酸,故C正确;
D.钠最外层一个电子,容易失去电子,具有强的还原性,可用于冶炼钛、锆、铌等金属,故D正确;
故选:A.
点评 本题考查了元素化合物的性质和用途,性质决定用途,明确氯化钙、二氧化氯、浓硫酸、钠的性质是解题关键,题目难度不大.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙烷、乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 | |
| B. | “酸可以除锈”,“洗涤剂可以去油”都是发生了化学变化 | |
| C. | 被蜂蚁蜇咬会感觉疼痛难忍,这是由于人的皮肤被注入了甲酸的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| D. | 苯酚皂溶液可用于环境消毒,医用酒精可用于皮肤消毒.其原因均在子可使蛋白质变性凝固 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子序数不可能为Z>Y>X | B. | X可能是非金属元素 | ||
| C. | Z一定在Y的下一周期 | D. | Y不可能在Z的下一周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| B. | 用量筒量取20 mL 0.5000 mol•L-1H2SO4溶液于烧杯中,加水80mL配制成0.1000mol•L-1H2SO4溶液 | |
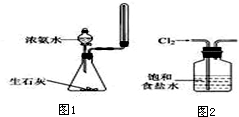
| C. | 实验室用图1所示装置制取少量氨气 | |
| D. | 实验室用图2所示装置除去Cl2中的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

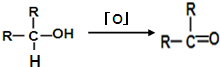
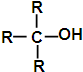
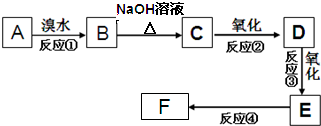

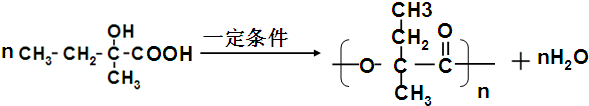
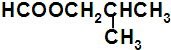 、
、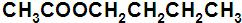 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将人群向高处疏散 | |
| B. | 将人群向顺风方向疏散 | |
| C. | 用浸有水或肥皂水(弱碱性)的毛巾捂住口鼻 | |
| D. | 向泄漏地点撒一些石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
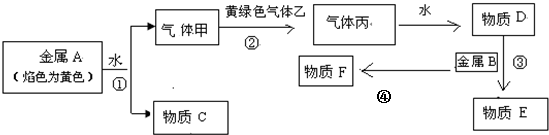
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体密度不再发生变化 | |
| B. | A的物质的量浓度不再改变 | |
| C. | 容器内总压强不再改变 | |
| D. | 单位时间内消耗4nmolA,同时消耗5nmolB |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知:0.4mol液态N2H4与足量的液体双氧水反应,生成氮气和水蒸气,放出200.0kJ的热量.
已知:0.4mol液态N2H4与足量的液体双氧水反应,生成氮气和水蒸气,放出200.0kJ的热量.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com