
| A. | 铝热反应发生时,火星四射并发出大量的热 | |
| B. | 将铜丝伸入浓硝酸中,产生红棕色气体 | |
| C. | 将二氧化硫通入品红溶液中,溶液褪色 | |
| D. | 氢气在氯气中燃烧,产生淡蓝色火焰 |
分析 A.铝热反应为放热反应,反应时火星四射并发出大量的热;
B.铜与浓硝酸反应生成红棕色的二氧化氮气体;
C.二氧化硫具有漂白性,能够使品红溶液图示;
D.氢气在氯气中燃烧产生苍白色火焰.
解答 解:A.铝热反应中放出大量热,反应剧烈,火星四射,故A正确;
B.将铜丝伸入浓硝酸中,反应生成硝酸铜、二氧化氮气体和水,所以产生红棕色气体,故B正确;
C.二氧化硫具有漂白性,将二氧化硫通入品红溶液中,溶液会褪色,故C正确;
D.氢气在氯气中燃烧产物苍白色火焰,生成HCl气体,还观察到白雾,故D错误;
故选D.
点评 本题考查常见元素及其化合物性质,为高频考点,把握物质的性质及发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 50g质量分数为17%的H2O2水溶液中含氧原子数目为0.5NA | |
| B. |  12g石墨烯(如图)中含有C-C键的数目为1.5NA 12g石墨烯(如图)中含有C-C键的数目为1.5NA | |
| C. | 常温下,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| D. | 一定量的Na2O2与H2O反应产生1.12L O2,则反应中转移的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaClO和NaCl混合溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O═HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液: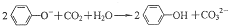 | |
| D. | 向明矾溶液中滴加Ba(OH)2溶液至溶液呈中性:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜插入稀硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+H2O | |
| B. | 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe=2Fe3+ | |
| C. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+3Na+ | |
| D. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3﹒H2O=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池是将电能转化为化学能的过程 | |
| B. | 煤燃烧是化学能转化为热能的过程 | |
| C. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| D. | 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23g Na 与足量H2O反应完全后可生成nA个H2分子 | |
| B. | 1 mol乙烯分子含有2nA碳碳双键 | |
| C. | 标况下,22.4LN2和H2混合气中含nA个原子 | |
| D. | 标况下,22.4LCl2与足量Fe和Cu混合物点燃,反应后,转移的电子数为2nA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
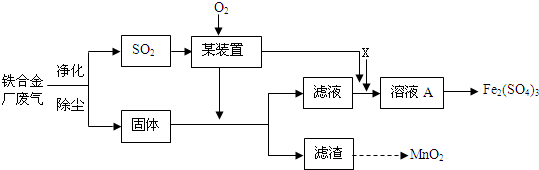
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com