
【题目】25℃时,向盛有50 mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是( )
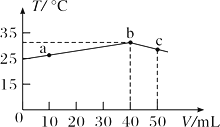
A. HA溶液的物质的量浓度为0.0l mol/L
B. a→b的过程中,混合溶液不可能存在:c(A-)=c(Na+)
C. b→c的过程中,温度降低的主要原因是溶液中A-发生了水解反应
D. 25℃时,HA的电离平衡常数K约为1.25×10—6
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】恒容条件下,1 mol SiHCl3发生如下反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
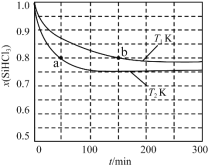
A. 该反应为放热反应,v正,a<v逆,b
B. T1 K时平衡体系中可通过移走SiCl4提高SiHCl3的转化率
C. 当反应进行到a处时,v正/v逆=16/9
D. T2 K时平衡体系中再充入1 mol SiHCl3,平衡正向移动,x(SiH2Cl2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷及其化合物与人们的健康和生产生活密切相关。请回答下列问题:
(1)基态磷原子价电子轨道表示式为___________,其第一电离能比硫的___________(填“大”或“小”)。
(2).羟基磷灰石[Ca(PO4)3OH]是牙齿中的重要矿物质,其中羟基(-OH)中氧原子的杂化方式为___________,PO43-的空间构型为___________,该化合物所含元素电负性最大的是___________。
(3)P4O6的分子结构中只含有单键,且每个原子的最外层都满足8电子结构,则该分子中含有的共价键数目是___________。
(4)磷酸和亚磷酸(H3PO3)是磷元素的两种含氧酸。亚磷酸与NaOH反应只生成NaHPO3和NaH2PO3两种盐,则H3PO3的结构式为___________,其为___________元酸,原因是___________。
(5)磷酸分子间脱水可生成多磷酸,其某一钙盐的结构如下图所示:
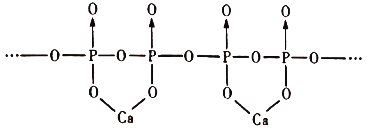
由图推知该多磷酸钙盐的通式为___________。
(6)磷化硼是一种超硬耐磨涂层材料,晶胞如下图所示,其密度为ρg/cm3,设NA是阿伏加德罗常数的值,则磷原子的配位数为___________,晶胞参数为___________pm。
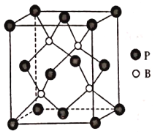
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将淀粉水解,并用新制Cu(OH)2悬浊液检验其水解产物的实验中,要进行的主要操作有:①加热;②滴入稀硫酸;③加入新制Cu(OH)2悬浊液;④加入足量的氢氧化钠溶液。以上操作步骤的先后顺序排列正确的是
A. ①②③④① B. ②①③④①
C. ②④①③① D. ②①④③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
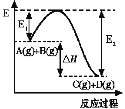
(1)该反应是_____________反应(填“吸热”或“放热”)。
(2)下列表述能作为反应达到化学平衡状态的标志是(________)
A.反应速率v(A)∶v(B)∶v(C)∶v(D) =1∶1∶1∶1
B.各组分的质量分数不再改变
C.混合气体的平均相对分子质量不再改变
II.某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)从开始至2min,Z的平均反应速率为________________;
(2)向其中充入1 mol He(g)(He不参加反应),化学反应速率____________(填“加快”“减慢”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )。
A. 原电池负极被氧化
B. 任何化学反应都能设计成原电池
C. 化学反应的速率和限度均可通过改变化学反应条件而改变
D. 化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与平衡移动原理无关的是
A. 向含酚酞的Na2CO3溶液中滴加BaCl2溶液,红色变浅
B. 加热MgCl2·6H2O固体最终得到Mg(OH)Cl
C. 将FeS2矿石粉碎更有利于焙烧制备SO2气体
D. NO2气体经过冷凝和加压成无色液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用KMnO4固体和浓盐酸反应制氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)![]() 2KCl+2MnCl2+5Cl2↑+8H2O。
2KCl+2MnCl2+5Cl2↑+8H2O。
(1)该反应中氧化剂是_____________,还原剂是__________________。
(2)若反应中有0.20 mol 电子发生转移,生成氯气的体积为____________(标准状况),被氧化的HCl的物质的量是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%,其余为氧。
(1)X的分子式是________。
(2)X能与金属钠反应放出氢气,则X结构中含有的官能团的名称为________。
(3)X与空气中的氧气在催化剂作用下反应生成了Y,该反应的化学方程式是_________,反应类型为________。
(4)X与高锰酸钾酸性溶液反应可生成Z,在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若184 g X和120 g Z反应生成132 g W,该反应的化学方程式为_________,其中X的转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com