
下列实验操作不能达到其对应目的的是
序号 | 实验内容 | 实验目的 |
A. | 向盛有10滴0.1 mol/L AgNO3溶液的试管中滴加0.1 mol/L NaCl溶液,至不再有沉淀生成,再向其中滴加0.1 mol/L Na2S溶液 | 证明AgCl沉淀能转化为溶解度更小的Ag2S沉淀 |
B. | 向2 mL甲苯中加入3滴KMnO4酸性溶液,振荡;向2mL己烷中加入3滴KMnO4酸性溶液,振荡 | 证明与苯环相连的甲基易被氧化 |
C. | 向Na2SiO3溶液中通入CO2 | 证明碳酸的酸性比硅酸强 |
D. | 在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜并加热 | 验证淀粉已水解 |
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:2014-2015学年陕西省西安市高三下学期一模理综化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.碳酸氢钾水【解析】
HCO3—+H2O  H3O++CO32—
H3O++CO32—
B.向硝酸银溶液中加入过量氨水:Ag++NH3·H2O=AgOH↓+NH4+
C.浓度均为0.1mol·L-1的氢氧化钡溶液与碳酸氢铵溶液等体积混合Ba2++2OH-+NH4++ HCO3—=BaCO3↓+NH3·H2O+H2O
D.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川一中高三第二次模拟考试 理综化学试卷(解析版) 题型:实验题
(15分)某化学课外活动小组通过实验研究NO2的性质:(已知:2NO2+2NaOH = NaNO3+NaNO2+H2O)
任务1:利用下图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。

(1)E装置中制取NO2反应的离子方程式是 。
(2)若NO2能够被NH3还原,预期观察到C装置中的现象是 。
(3)实验过程中,未能观察到C装置中的预期现象。该小组同学从反应原理的角度分析了原因,认为可能是:①NH3还原性较弱,不能将NO2还原;②在此条件下,NO2的转化率极低;③ 。
(4)此实验装置存在一个明显的缺陷是 。
任务2:探究NO2能否与Na2O2发生氧化还原反应。
(5)实验前,该小组同学提出三种假设。
假设1:二者不反应;
假设2:NO2能被Na2O2氧化;
假设3: 。
(6)为了验证假设2,该小组同学选用任务1中的B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如图所示),重新组装,进行实验。
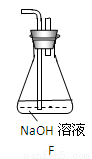
①装置的合理连接顺序是(某些装置可以重复使用) 。
②实验过程中,B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成。推测B装置中反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高三上学期第五次模拟考试理综化学试卷(解析版) 题型:选择题
下列装置进行的相应实验,能达到实验目的的是
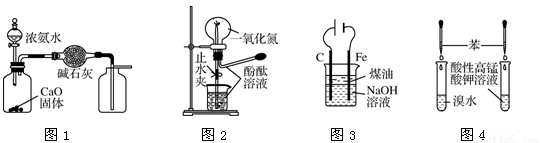
A.用图1装置制取并收集干燥纯净的NH3
B.用图2装置可演示NO的喷泉实验
C.用图3装置制备Fe(OH)2并能较长时间观察其颜色
D.用图4装置验证苯中是否有独立的碳碳双键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三5月一模化学试卷(解析版) 题型:简答题
(13分)SO2、NO是大气污染物。吸收SO2 和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中生成HSO3-的离子方程式为 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图所示。

①下列说法正确的是 (填字母序号)。
a.pH=8时,溶液中c(HSO3-) < c(SO32-)
b.pH=7时,溶液中c(Na+) =c(HSO3-)+c(SO32-)
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式 。
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
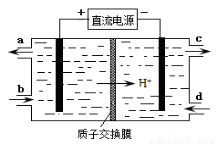
①生成Ce4+的电极反应式为 。
②生成Ce4+从电解槽的 (填字母序号)口流出。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L(用含a代数式表示,计算结果保留整数).
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省等高三下学期期中四校联考化学试卷(解析版) 题型:填空题
(A)(13分)在晶体中,微观粒子是有规律排布的。而实际上的晶体与理想结构或多或少会产生偏离,这种偏离称为晶体的缺陷。由于晶体缺陷,氧化铁FexO中的x常常不确定。
(1)请写出铁原子基态电子排布式 。
(2)Fe2+与Fe3+相比,较稳定的是 ,请从二者结构上加以解释 。
(3)硫氰根离子和异硫氰根离子都可用SCN-表示,碳原子都处于中央,则碳原子的轨道杂化类型为 。其中异硫氰根离子与CO2是等电子体,异硫氰根离子的电子式为 。Fe3+与SCN―可以形成配位数1~6的配离子,若Fe3+与SCN―以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为 。
(4)如图:铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法不正确的是
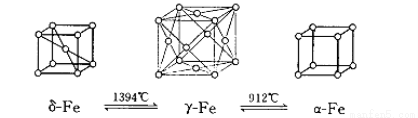
A.γ-Fe晶体中,铁原子的配位数为12
B.δ-Fe晶体和α-Fe晶体都是非密置在三维空间堆积而成的,堆积后非密置层都保持原来的结构不变
C.三种晶体的空间利用率大小为:γ-Fe晶体>δ-Fe晶体>α-Fe晶体
D.三种晶胞的棱长之比为: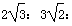 3
3
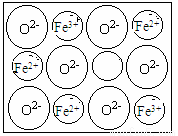
(5)FexO有NaCl结构的晶胞。今有某种FexO晶体中就存在如图所示的缺陷,其密度为5.71 g·cm-3,晶胞棱长为a=4.28×10-8cm(已知:4.283=78.4),则x= 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省等高三下学期期中四校联考化学试卷(解析版) 题型:选择题
常温下用惰性电极电解1 L含足量KCl的溶液,若通过n mol电子的电量,则溶液的pH与n的关系是(设电解前后溶液的体积不变,生成的气体全部逸出)
A.pH=n B.pH=-lg n C.pH=14-lgn D.pH=lgn+14
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省等高三下学期期中四校联考化学试卷(解析版) 题型:选择题
化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是
A.将草木灰和硫铵混合使用,相当于施用了氮和钾的复合肥料,提高了肥料利用率
B.铝制容器不能长期盛装酸性或碱性食品,但可用于长期盛放腌制食品
C.氟里昂(CCl2F2)或NOx都可以破坏臭氧层,从而导致了“温室效应”
D.大量使用含磷洗涤剂,可导致水体富营养化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期三调考试化学试卷(解析版) 题型:简答题
选考[化学——化学与技术](15分)往有机聚合物中添加阻燃剂,可增加聚合物的使用安全性,扩大其应用范围。Mg(OH)2是一种常用的阻燃剂,生产工艺如下:

完成下列填空:
(1)精制卤水中MgCl2的与适量石灰乳反应合成碱式氯化镁 ,反应的化学方程式为_________。
,反应的化学方程式为_________。
(2)合成反应后,继续在393K~523K下水热处理8h,发生反应:
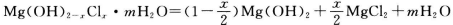 ,水热处理后,进行过滤、水洗。水洗的目的是_________。
,水热处理后,进行过滤、水洗。水洗的目的是_________。
(3)阻燃型 Mg(OH)2具有晶粒大,易分散、与高分子材料相容性好等特点。上述工艺流程中与此有关的步骤是________。
(4)已知热化学方程式: 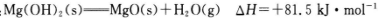
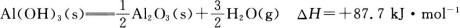
Mg(OH)2和Al(OH)3起阻燃作用的主要原因是_________。
等质量 Mg(OH)2和Al(OH)3 相比,阻燃效果较好的是_________,原因是____________________。
(5)该工业生产的原料还可以用来提取金属镁。请设计提取金属镁的工艺流程(框内写产物名称,箭头上标明转化条件):
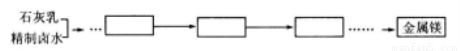
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com