
| 族 周期 | IA | IIA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
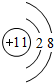 ,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.分析 (1)(2)由元素在周期表中位置,可知①为C、②为N、③为O、④为F、⑤为Na、⑥为Mg、⑦为Al、⑧为Si、⑨为P、⑩为S、⑪为Cl、⑫为Ar;
(3)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱.稀有气体的化学性质最不活泼;
(4)这些元素的最高价氧化物对应水化物中,高氯酸的酸性最强,氢氧化钠的碱性最强;氢氧化铝是能形两性氢氧化物;
(5)同周期自左而右原子半径减小;
(6)同周期自左而右金属性减弱,单质活泼性减弱,可以利用单质与水的反应剧烈程度等进行验证.
解答 解:由元素在周期表中位置,可知①为C、②为N、③为O、④为F、⑤为Na、⑥为Mg、⑦为Al、⑧为Si、⑨为P、⑩为S、⑪为Cl、⑫为Ar.
(1)①、②两种元素的名称分别为:碳、氮,故答案为:碳;氮;
(2)⑧、⑨两种元素的符号分别为:Si、P,故答案为:Si;P;
(3)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,在这些元素中,最活泼的金属为Na,离子结构示意图是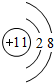 ,最活泼的非金属元素是F元素,Ar是最不活泼的元素,
,最活泼的非金属元素是F元素,Ar是最不活泼的元素,
故答案为: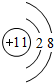 ;F;Ar;
;F;Ar;
(4)这些元素的最高价氧化物对应水化物中,HClO4的酸性最强,NaOH的碱性最强;氢氧化铝是能形两性氢氧化物,
故答案为:HClO4;NaOH;Al;
(5)同周期自左而右原子半径减小,故原子半径Cl原子半径最小,故答案为:Cl;
(6)同周期自左而右金属性减弱,故单质活泼性Na>Mg,用实验证明方案为:金属钠与金属镁单质分别与冷水反应,反应剧烈程度大的是钠,反之是镁,
故答案为:Na;金属钠与金属镁单质分别与冷水反应,反应剧烈程度大的是钠,反之是镁.
点评 本题考查元素周期表与元素周期律,熟练掌握元素周期表的结构,注意金属性、非金属性强弱比较实验事实.


科目:高中化学 来源: 题型:选择题
| A. | X、Y的单质均具有较高的熔沸点 | |
| B. | Z、W形成的化合物中既含有离子键,有含有共价键 | |
| C. | 原子半径由大到小的顺序:X、Y、Z | |
| D. | 最高价氧化物对应水化物的酸性由强到弱的顺序:W、Y、X |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C |
| D | E | F |
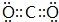 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 实验 编号 | 温度 /℃ | 平衡常数 /mol-1•L | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| SO2 | O2 | SO2 | O2 | ||||
| 1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
| A. | x=2.4 | |
| B. | T1、T2的关系:T1>T2 | |
| C. | K1、K2的关系:K2>K1 | |
| D. | 实验1在前6 min的反应速率v(SO2)=0.2 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
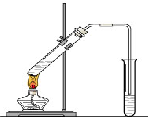 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: CH3COOC2H5+H2O
CH3COOC2H5+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
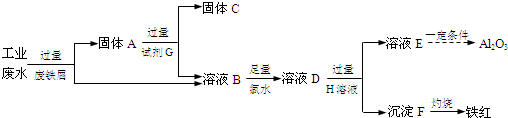
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
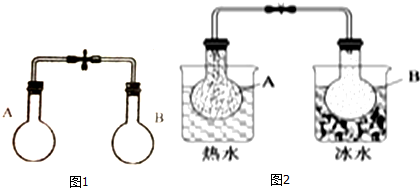
| A. | 图2中,B烧瓶颜色较深 | |
| B. | 图2中,B烧瓶与A烧瓶相比有较多的NO2 | |
| C. | 图2中B烧瓶的正反应速率比图1中B烧瓶的快 | |
| D. | 图2中A烧瓶的正反应速率比图1中A烧瓶的快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com