
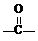 OH$\stackrel{SOCl_{2}}{→}$R
OH$\stackrel{SOCl_{2}}{→}$R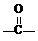 Cl
Cl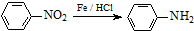
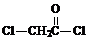 ,⑥的反应类型是取代反应.
,⑥的反应类型是取代反应. .
.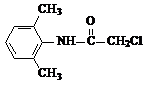 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$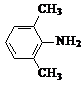 +HOCH2COONa+NaCl.
+HOCH2COONa+NaCl.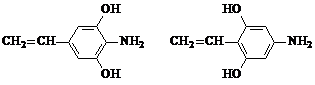 .
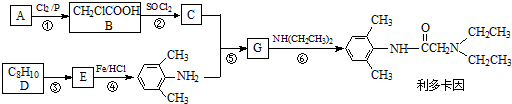
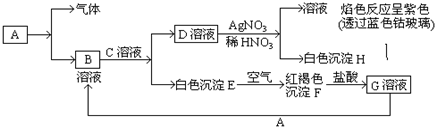
.分析 A发生取代反应生成B,根据B结构简式知,A结构简式为CH3COOH,B发生取代反应生成C,结合题给信息知,C结构简式为CH2ClCOCl,D反应生成E,E发生反应④,结合题给信息知,E结构简式为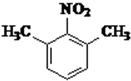 ,D发生取代反应生成E,D结构简式为
,D发生取代反应生成E,D结构简式为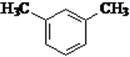 ,G发生取代反应生成利多卡因,则G结构简式为
,G发生取代反应生成利多卡因,则G结构简式为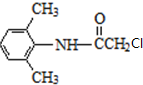 ,反应⑥为取代反应,据此分析解答.
,反应⑥为取代反应,据此分析解答.
解答 解:A发生取代反应生成B,根据B结构简式知,A结构简式为CH3COOH,B发生取代反应生成C,结合题给信息知,C结构简式为CH2ClCOCl,D反应生成E,E发生反应④,结合题给信息知,E结构简式为 ,D发生取代反应生成E,D结构简式为
,D发生取代反应生成E,D结构简式为 ,G发生取代反应生成利多卡因,则G结构简式为
,G发生取代反应生成利多卡因,则G结构简式为 ,反应⑥为取代反应,
,反应⑥为取代反应,
(1)A中甲基上C原子价层电子对个数是4、羧基上的C原子价层电子对个数是2,所以C原子采用杂化方式为sp3、sp2杂化,D名称是1,3-二甲苯(或间二甲苯),故答案为:sp3、sp2杂化;1,3-二甲苯(或间二甲苯);
(2)通过以上分析知,C结构简式为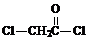
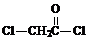
(3)该反应方程式为 ,故答案为:
,故答案为: ;
;
(4)G结构简式为 ,G和NaOH水溶液反应方程式为
,G和NaOH水溶液反应方程式为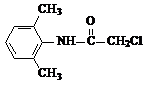
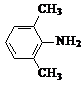
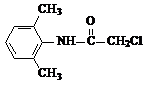
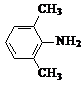
(5)E结构简式为 ,E的同分异构体符合下列条件:a.能使Br2的CCl4溶液褪色,遇FeCl3溶液显色,说明含有不饱和键和酚羟基;
,E的同分异构体符合下列条件:a.能使Br2的CCl4溶液褪色,遇FeCl3溶液显色,说明含有不饱和键和酚羟基;
b.含有-NH2,苯环上只有1种氢,符合条件的同分异构体结构简式为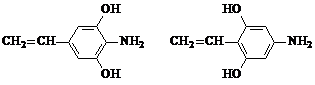
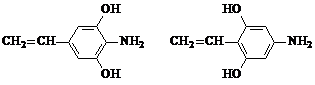
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力及获取信息利用信息解答问题能力,根据某些物质结构简式结合反应条件、题给信息进行推断,正确判断各物质结构简式是解本题关键,难点是同分异构体种类判断,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 0.9gH2O中含有电子数为NA | |
| B. | 11.2 LCl2中含有的原子数为NA | |
| C. | 常温常压下,48gO2和O3含有的氧原子数均为3NA | |
| D. | 标准状况下,11.2L CCl4所含的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| B. | SO2和Na2SO3溶液都能使氯水褪色 | |
| C. | 常温下铁和铂都不溶于浓硝酸 | |
| D. | 硫化钠和亚硫酸钠固体长期暴露在空气中变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+ AlO2- | B. | Na+ SO42- | C. | Cu2+ SO42- | D. | Na+ CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  反应过程中能量关系可用图表示 | |
| B. | 该反应为自发反应 | |
| C. | 若将该反应设计成原电池则锌为负极 | |
| D. | 若将其设计为原电池,当有32.5g锌溶解时,正极放出气体为11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com