
六氟化硫分子为正八面体构型(分子结构如图所示),难溶于水,有良好的绝缘性、阻燃,在电器工业方面具有广泛用途。下列推测正确的是( )
A.SF6中各原子均达到8电子稳定结构
B.SF6二氯取代物有3种
C.SF6分子是含有极性键的非极性分子
D.SF6是原子晶体

科目:高中化学 来源: 题型:
(1)已知下列两个热化学方程式:
C3H8(g)+5O2(g) 3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1
H2O(l) H2O(g) ΔH=+44.0 kJ·mol-1
则0.5 mol丙烷燃烧生成CO2和气态水时释放的热量为___________ 。
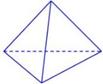
(2)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如下图所示),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN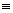 N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________ kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________ kJ能量。
(3)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:
2H2+O2 2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将___能转化为____能。其电极反应式分别为:负极________________,正极__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)AgNO3的水溶液呈酸性的原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,充分反应后溶液呈中性,则反应后溶液存在的离子有 ,其浓度由大到小的顺序为 ,氨水的浓度a 0.01 mol·L-1(填“>”、“ <”或“=”)。
(3)用已知浓度的NaOH标准溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是
A.未用标准液润洗碱式滴定管;
B.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
D.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
查看答案和解析>>
科目:高中化学 来源: 题型:
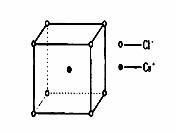
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为:
A. 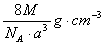 B.
B.
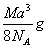
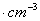
C. 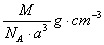 D.
D. 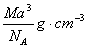
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成形成YM3分子;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是( )
A.原子半径:W>Z>Y>X>M
B.XZ2、X2M2、W2Z2均为直线型的共价化合物
C.由X元素形成的单质不一定是原子晶体
D.由Y、Z、M三种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是
A.Na+、Ca2+、Cl-、SO42- B.Fe2+、H+ 、SO32-、ClO-
C.Mg2+、NH4+、Cl- 、SO42- D.K+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组用甲、乙两套装置(如下图所示)进行甲酸(HCOOH)与甲醇(CH318OH)酯化反应的实验,回答以下问题:
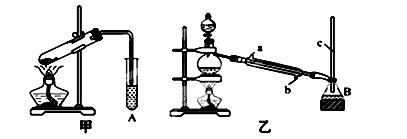
(1)甲酸(HCOOH)和甲醇(CH318OH)进行酯化反应的化学方程式是:
___ _。
(2)乙装置中长玻璃导管c的作用是__ ___。
(3)甲、乙两套装置中效果比较好的装置是 ,原因:
(4)试管A和锥形瓶B内装的是 :作用为
。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学的发展,把越来越多的高分子材料带进我们的生活。下列说法正确的是
A.热固性塑料具有线型结构
B.天然橡胶经过硫化后可提高其强度
C.尼龙、棉花等都是天然纤维
D.有机玻璃受热时会软化,易于加工成型,是一种硅酸盐材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com