
【题目】图像能直观地反映有关物理量的变化及规律,下列各图像与描述相符的是

A. 图1表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化
B. 图2表示0.lmolMgCl2·6H2O在空气中充分加热时固体质量随时间的变化
C. 图3表示分别稀释10 mL pH=2的盐酸和醋酸时溶液pH的变化,图中b>l00
D. 图4表示平衡2NO2(g)![]() N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化
N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化
科目:高中化学 来源: 题型:
【题目】向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法正确的是( )
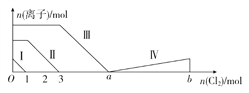
A. 线段Ⅱ表示Br-的变化情况 B. 线段Ⅳ表示IO3-的变化情况
C. 根据图象无法计算a的值 D. 原溶液中n(FeI2)∶n(FeBr2)=3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO4·7H2O用作天然水净化混凝剂,要调到pH为9左右的主要原因是( )
A.Fe2+在碱性条件下易被氧化成Fe3+
B.FeSO4·7H2O溶于水后显酸性
C.FeSO4·7H2O溶于水后显碱性
D.以上都不对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学完成如下探究实验:
实验目的:比较Cl2、Br2、I2三种单质的氧化性强弱
实验药品:NaBr溶液、KI溶液、氯水、淀粉溶液
实验记录:
实验步骤 | 实验现象 | 实验结论 |
| 溶液变为黄色 | 氧化性:Cl2>Br2 |
| 溶液变为黄色 | 氧化性: |
| 溶液的颜色由黄色变为蓝色 |
反思与评价:
(1)步骤①反应的离子方程式为: .
(2)检验②中所得黄色溶液含I2的另一种方法是(简述实验操作和相应的实验现象)
.
(3)你认为上述实验设计(填“能”或“不能”)达到实验目的,理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室合成了一种可溶的金属氯化物(RClx),为了测定该金属氯化物的成分,研究人员做了以下实验:取物质的量浓度为0.05molL﹣1的金属氯化物(RClx) 溶液20mL,使之恰好与20mL 0.15molL﹣1的AgNO3溶液完全反应.则该氯化物的化学式为( )
A.RCl
B.RCl2
C.RCl3
D.RCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组化合物中,化学键类型完全相同的是( )
A. HCl和NaOH B. Na2O和Na2O2
C. CO2和CS2 D. Ca(OH)2,和Na2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以烃A为主要原料,采用以下路线合成药物X和高聚物Y:

已知: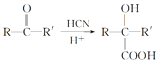 (R或R′可以是烃基或H原子)。
(R或R′可以是烃基或H原子)。
请回答下列问题:
(1)X的分子式为____________,X中的含氧官能团有____________。
(2)若反应①、反应②的原子利用率均为100%,则A的名称为________。
(3)E的结构简式为________________,反应③的条件是________,反应⑤的反应类型是________。
(4)写出反应④的化学方程式: ___________________________________。
(5)写出同时符合下列条件的E的所有同分异构体的结构简式:________。
①属于酚类化合物,且是苯的对位二元取代物;
②能发生银镜反应和水解反应。
(6)以CH3CHO为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com