
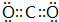 ,
,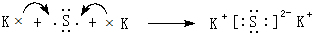 ,
,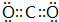 ;
;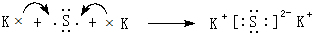 ;
;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 城市 | 污染 指数 |
首要 污染物 |
空气质 量级别 |
城市 | 污染 指数 |
首要 污染物 |
空气质 量级别 |
| 北京 | 92 | TSP | Ⅱ | 济南 | 76 | TSP | Ⅱ |
| 天津 | 82 | TSP | Ⅱ | 武汉 | 83 | NOx | Ⅱ |
| 长春 | 103 | TSP | Ⅲ | 深圳 | 77 | NOx | Ⅱ |
| 上海 | 74 | NOx | Ⅱ | 汕头 | 54 | Ⅱ | |
| 杭州 | 67 | TSP | Ⅱ | 成都 | 87 | TSP | Ⅱ |
| 福州 | 42 | Ⅰ | 重庆 | 98 | SO2 | Ⅱ | |
| 厦门 | 25 | Ⅰ | 贵阳 | 69 | TSP | Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B、0.1mol丙烯酸中含有双键的数目为0.1NA |
| C、标准状况下,11.2L苯中含有分子的数目为0.5NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com