
【题目】NaCl是我们生活中必不可少的物质,将NaCl晶体溶于水,其溶解过程示意图如图所示,下列说法正确的是( )
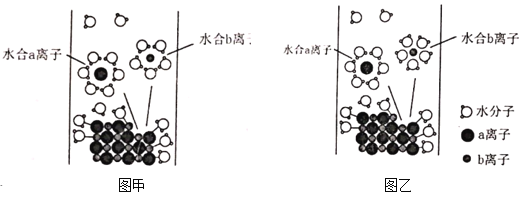
A.对比甲、乙两图,图甲中水合b离子的结构示意图不科学
B.图中a离子为![]() 、b离子为
、b离子为![]()
C.氯化钠晶体中存在离子键和分子间作用力
D.水分子对氯化钠晶体表面离子的作用不可能克服离子键的作用
【答案】A
【解析】
根据离子半径的大小,a离子的离子半径大于b离子的离子半径,推断出a离子是氯离子,b离子是钠离子,氯离子属于阴离子,吸引阳离子,钠离子属于阳离子,吸引阴离子,同时氯化钠属于离子晶体,只含有离子键,根据图中氯化钠溶于水后发生了电离,可知破坏了离子键。
A.图甲中水合b离子的结构示意图不科学,b离子是钠离子,属于阳离子,距离它较近的应该是氧原子而不是氢原子,A项正确;
B.根据离子半径大小推断出a离子为![]() 、b离子为
、b离子为![]() ,B项错误;
,B项错误;
C.氯化钠晶体中存在离子键,不存在分子间作用力,因为分子间作用力只存在于分子之间,而氯化钠是离子化合物,由离子构成,没有分子,C项错误;
D.根据图中所示,水分子对氯化钠晶体表面离子的作用克服离子键的作用,使氯化钠发生了电离,D项错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,在一定的条件下,它们之间具有如下转化关系:![]() 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2B.若甲为Fe,则丁可能是氯气
C.若甲为Fe,则丁可能是硝酸D.若甲为NaOH 溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲![]() 乙
乙![]() 丙。下列有关物质的推断错误的是[已知Al3++3AlO2-+6H2O=4Al(OH)3↓]
丙。下列有关物质的推断错误的是[已知Al3++3AlO2-+6H2O=4Al(OH)3↓]
A.若甲为焦炭,则丁可能是O2
B.若甲为AlCl3溶液,则丁可能是KOH溶液
C.若甲为Cu,则丁可能是Cl2
D.若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是
A.1molMgCl2中含有的离子数为2NA
B.标准状况下,11.2LH2O中含有的原子数为1.5NA
C.标准状况下,22.4L氦气与22.4L氯气所含原子数均为2NA
D.常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为组成人体细胞的主要的元素及其比例。下列相关叙述中,错误的是( )

A.图中所示为细胞鲜重中主要的元素的所占比例
B.因为 O 的含量最多,所以 O 是构成有机物的最基本元素
C.细胞失去大部分水分后,C 的所占比例最大
D.图中所示的元素在非生物界也可以找到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应![]() 在容积为10L的密闭容器中进行。起始时
在容积为10L的密闭容器中进行。起始时![]() 和
和![]() 均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法不正确的是( )
均为0.20mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。下列说法不正确的是( )

A. 实验c条件下,从反应开始至达到平衡时![]()
B. 实验a条件下,用浓度表示的平衡常数为100
C. 该反应的![]()
D. 比较实验a、c可判断升高温度反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别物质的方法中,不正确的是( )
A.用KSCN溶液鉴别FeCl2和FeCl3溶液
B.用澄清石灰水鉴别NaHCO3和Na2CO3
C.用焰色反应鉴别NaCl溶液和KCl溶液
D.用过量的NaOH溶液鉴别AlCl3溶液和MgCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:

(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H-除外):_________________________,Mg在元素周期表中的位置:_____________________,Mg(OH)2的电子式:____________________。
(2)A2B的化学式为_______________。反应②的必备条件是_______________。上图中可以循环使用的物质有_______________。
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料_______________(写化学式)。
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:_______________。
(5)用Mg制成的格氏试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
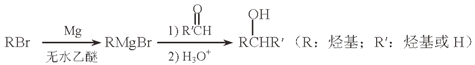
依据上述信息,写出制备![]() 所需醛的可能结构简式:_______________。
所需醛的可能结构简式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸雨形成的原理之一可表示如下:
含硫燃料![]() A
A![]() B
B![]() 硫酸
硫酸
请回答下列问题。
(1)A的化学式为__________,B的化学式为__________________________________。
(2)三个反应中,不属于氧化还原反应的是________(填序号)。
(3)SO2中硫元素显+4价,它可以降低到0价,利用这一性质可在工厂的烟道气中通入合适的________(填“氧化剂”或“还原剂”)除去SO2,达到减少污染的目的。
(4)雨水的pH小于5.6时,就判定为酸雨。已知pH=-lgc(H+),经测定某次雨水所含酸性物质只有硫酸,且其浓度为5×10-5mol·L-1,则这次降雨________(填“是”或“不是”)酸雨。
(5)火力发电厂燃烧的煤中含有大量的硫,其排出的废气中往往含有SO2、CO2等。为了除去有害的SO2气体,在英国已进行了一个研究,结果表明:高烟囱可以有效降低地面SO2的浓度。在20世纪60年代到70年代的10年间,由发电厂排放的SO2增加了35%,但由于高烟囱的建造,地面SO2浓度降低了30%之多。
①你认为减少酸雨产生可采取的措施是__________(填字母)。
A.少用煤作燃料 B.把工厂的烟囱建高
C.燃料脱硫 D.把工厂迁移到农村
E.开发新能源
②请从全球环境保护的角度,分析这种建高烟囱的方法是否可取?________(填“可取”或“不可取”),理由是__________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com