
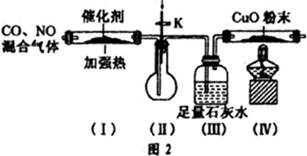
 CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为
CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为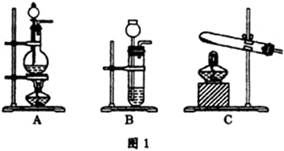
| 沉淀物 | Fe(OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A + B | 无明显现象 |
| ② | B + D | 有无色无味气体放出 |
| ③ | C + B | 有白色沉淀生成 |
| ④ | A + D | 有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲溶液含有SO42- | B.乙溶液含有SO42- |
| C.丙溶液显酸性 | D.丁溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
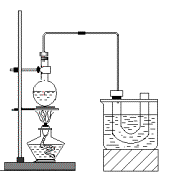
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
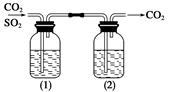
| A.(1)NaOH;(2)浓H2SO4 | B.(1)浓H2SO4;(2)NaOH |
| C.(1)NaHCO3;(2)浓H2SO4 | D.(1)浓H2SO4;(2)Na2CO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.实验室制备乙酸乙醋时,往浓硫酸中缓慢加入乙醇和冰醋酸的混合液 |
| B.实验室制备干燥纯净的氯气时,气体先通过饱和食盐水再通过浓硫酸 |
| C.检验溶液中C1一和SO42-,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液 |
| D.检验FeC12溶液中Fe2+先加入氯水再滴加少量KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
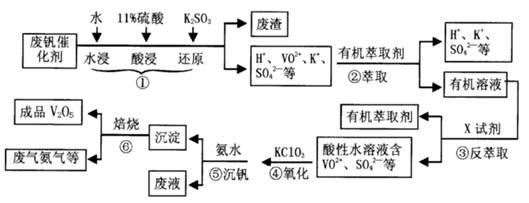
 2RAn(有机层) + nH2SO4 (水层)为提高②中萃取百分率,应采取的措施是 。
2RAn(有机层) + nH2SO4 (水层)为提高②中萃取百分率,应采取的措施是 。| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
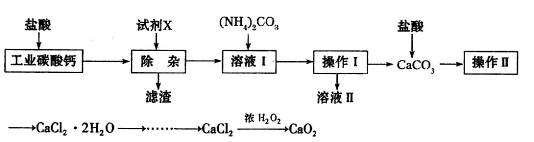
| A.CaO | B.CaCO3 | C.NH3·H2O | D.Ba(OH)2 |
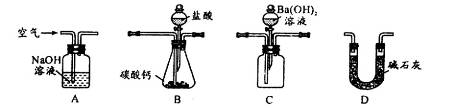
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com