
下列操作或说法正确的是( )
A.乙醇可作为提取碘水中碘的萃取剂
B.除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层
C.加入过量浓溴水除去苯中混有的少量苯酚
D.分离乙二醇和丙三醇应采用分液的方法
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
如图是制备和研究乙炔性质的实验装置图。下列说法不正确的是( )
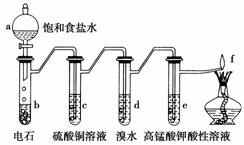
A.制备乙炔的反应原理是CaC2+2H2O―→Ca(OH)2+C2H2↑
B.c的作用是除去影响后续实验的杂质
C.d中的有机产物与AgNO3溶液混合能产生沉淀
D.e中的现象说明乙炔能被高锰酸钾酸性溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
|
| A. | 乙酸乙酯和水,酒精和水,植物油和水 |
|
| B. | 四氯化碳和水,溴苯和水,硝基苯和水 |
|
| C. | 甘油和水,乙酸和水,乙酸和乙醇 |
|
| D. | 汽油和水,苯和水,乙酸和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在比较酸的强弱时,必须考虑两方面:一是电离出氢离子的能力,二是溶剂接受氢离子的能力.比如HCl在水中是强酸,在冰醋酸中就是弱酸;而HAc在水中是弱酸,在液氨中却是强酸,就是因为接受氢离子的能力:NH3>H2O>HAc.下列关于酸性强弱的说法正确的是( )
|
| A. | 在A溶剂中,甲的酸性大于乙;在B的溶剂中,甲的酸性可能小于乙 |
|
| B. | 比较HCl、H2SO4、HClO4、HNO3酸性的强弱,用水肯定不可以,用冰醋酸可能可以 |
|
| C. | HNO3在HClO4中是酸,在H2SO4中可能是碱 |
|
| D. | 比较HCN与HAc酸性的强弱,用水肯定可以,用液氨肯定也可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:
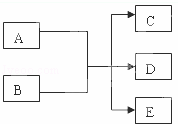
在一定条件下,某些化学反应可以用如图框架表示,根据要求回答下列问题:
(1)若A、C、D均为含氯物质,且A的化合价介于C和D之间,D具有漂白性,写出该反应的离子方程式 ;
(2)若通过电解的方法获得黄绿色气体C,则该反应的离子方程式为
(3)若C、D均为气体且均能使澄清石灰水变浑浊,写出符合上述框图要求的化学方程式
(4)若A为红色金属单质,B为第二周期某种元素的最高价氧化物的水化物的稀溶液,写出符合上述框图关系的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示。下列叙述正确的是( )
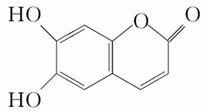
A.M的相对分子质量是180
B.1 mol M最多能与2 mol Br2发生反应
C.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4
D.1 mol M与足量NaHCO3反应能生成2 mol CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.实验室制NH3:NH +OH-
+OH-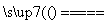 NH3↑+H2O
NH3↑+H2O
B.NaOH与NH4Cl溶液混合加热:NH +OH-
+OH-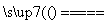 NH3·H2O
NH3·H2O
C.氨水中加盐酸:NH3·H2O+H+===NH +H2O
+H2O
D.氨气通入稀H2SO4中:NH3+H+===NH
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
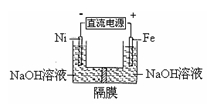
A.铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+
B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
C.若隔膜为阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能存在的数据是 ( )
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能存在的数据是 ( )
A.SO2为0.4 mol·L-1、O2为0.2 mol·L-1
B.SO2为0.25 mol·L-1
C.SO2、SO3均为0.15 mol·L-1
D.SO3为0.4 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com