
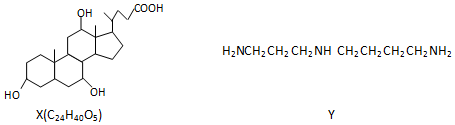
| A. | 1molX在浓硫酸作用下发生消去反应,最多生成3molH2O | |
| B. | 1molY发生类似酯化的反应,最多消耗2molX | |
| C. | X与足量HBr反应,所得有机物的分子式为C24H37O2Br3 | |
| D. | Y与癸烷的分子链均呈锯齿形,但Y的极性较强 |
分析 A.1个分子中含3个-OH,能发生消去反应;
B.-NH2与-COOH可发生反应;
C.-OH能与HBr发生取代反应,-OH被-Br替代;
D.Y和癸烷均存在饱和烃结构,Y中含-NH2,极性增强.
解答 解:A.1个分子中含3个-OH,能发生消去反应,则1mol X在浓硫酸作用下发生消去反应,最多生成3mol H2O,故A正确;
B.-NH2与-COOH可发生反应,则1mol Y发生类似酯化的反应,最多消耗3mol X,故B错误;
C.-OH能与HBr发生取代反应,-OH被-Br替代,则X与足量HBr反应,所得有机物的分子式为C24H37O2Br3,故C正确;
D.Y和癸烷均存在饱和烃结构,所以分子链均呈锯齿形,Y中含-NH2,极性Y比癸烷强,故D正确;
故选B.
点评 本题考查有机物的结构与性质,明确常见有机物的性质即可解答,注意把握有机物的官能团与性质的关系来解答,题目难度不大.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 将苯加入溴水中振荡后,水层接近无色,是因为发生了取代反应 | |
| B. | 1 体积某气态烃与 HC1 充分加成消耗 HC11体积,加成后的物质最多还能和 5 体 积氯气发生取代反应,由此推断原气态烃是乙烯 | |
| C. | 乙醇与钠、氢氧化钠溶液均反应 | |
| D. | 等质量的乙烯和乙醇在氧气中充分燃烧后耗氧量相同. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1 mol亮菌甲素与溴水反应最多消耗3 mol Br2 | |
| B. | 分子中所有碳原子不可能共平面 | |
| C. | 1 mol亮菌甲素在一定条件下与NaOH溶液完全反应最多能消耗2 mol NaOH | |
| D. | 1 mol亮菌甲素在一定条件下可与6 mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酯化反应也属于加成反应 | |
| B. | 酯化反应中羧酸脱去羧基中的氢原子,醇脱去羟基中的羟基生成水 | |
| C. | 浓硫酸在酯化反应中不只起催化剂的作用 | |
| D. | 欲使酯化反应生成的酯分离并提纯,可以将酯蒸气通过导管伸入饱和碳酸钠溶液的液面下,再用分液漏斗分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,另外一种生成物的化学式为Na2MoO4
,另外一种生成物的化学式为Na2MoO4查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ③④②①⑥⑤ | C. | ①④③②⑥⑤ | D. | ①③④②⑥⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应开始时,盐酸与锌反应放出氢气的速率更快 | |
| B. | 盐酸和醋酸分别与锌完全反应所需时间一样长 | |
| C. | 醋酸与锌反应放出的氢气多 | |
| D. | 盐酸和醋酸分别与锌反应放出的氢气一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个D2O分子中,含有10NA个电子 | |
| B. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为6NA | |
| C. | 1.2g金刚石与石墨的混合物这含有碳碳单键的数目为0.4NA | |
| D. | 1molCl2与足量铁反应转移的电子数目为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com