
一定温度下,反应X(g)+3Y(g)⇌2Z(g)达到化学平衡状态的标志是( )
|
| A. | X、Y、Z的分子数比为1:3:2 |
|
| B. | 单位时间生成amolX,同时生成3a molY |
|
| C. | X、Y、Z的浓度相等 |
|
| D. | 3v正(X)=v逆(Y) |
考点:
化学平衡状态的判断.
专题:
化学平衡专题.
分析:
根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、X、Y、Z的分子数比可能为1:3:2,也可能不是1:3:2,与各物质的初始浓度及转化率有关,当反应达到平衡状态时,正逆反应速率相等,但不为0,故A错误;
B、单位时间生成amolX,同时生成3a molY都体现的逆向,故B错误;
C、当体系达平衡状态时,X、Y、Z的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故C错误;
D、3v正(X)=v正(Y)=v逆(Y),故D正确;
故选D.
点评:
本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1价和+2价的化合物。
(1)写出基态Cu+的核外电子排布式___________________________________。
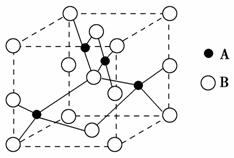 (2)如图是铜的某种氧化物的晶胞示意图,该氧化物的化学式为________。
(2)如图是铜的某种氧化物的晶胞示意图,该氧化物的化学式为________。
(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀,该物质中的NH3通过________键与中心离子Cu2+结合,NH3分子中N原子的杂化方式是____。与NH3分子互为等电子体的一种微粒是________。
(4)CuO的熔点比CuCl的熔点____(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某主族元素R的最高化合价与负化合价代数和为6.下列说法正确的是()
A. R的气态氢化物能燃烧
B. R的最高价氧化物为RO3
C. R一定是第ⅦA族元素
D. R的气态氢化物易溶于水显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列观点中,错误的是()
A. 化学反应既能实现物质的转化、又能实现能量的转化
B. 分子是保持物质化学性质的一种粒子
C. 储存在物质中的化学能在化学反应前后是不变的
D. 构成宏观物质的微观粒子之间的相互作用有多种形式,如离子键、共价键等
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物,A的单质常温下为密度最小的气体;B与Z的最外层电子数之比为2:3,常见化合物Y2X2是淡黄色固体,能与水反应生成X的单质,其溶液可使酚酞试液变红.请回答下列问题.
(1)Y的原子结构示意图为; Z在周期表中的位置是;B元素的名称为碳.
(2)化合物Y2X2属于A(填序号).
A.离子化合物 B.共价化合物
(3)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为.
(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入(填物质名称);放电时KOH溶液中的OH﹣往负极方向移动(填正或负).
(5)1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h行驶了40km.为了有效发展民用氢能源,首先必须制得廉价的氢气.下列可供开发、较经济又具有广阔前景的制氢方法是(填写编号)
①光解海水 ②锌和稀硫酸反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42﹣)>c(NH4+) |
|
| B. | 两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 |
|
| C. | pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合,滴入石蕊溶液呈红色 |
|
| D. | 向0.1mol•L﹣1的氨水中加入少量硫酸铵固体,则溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
当下列各组物质的总物质的量不变时,使各组分以任意比混合后充分燃烧,消耗氧气的量和生成CO2的物质的量不变的是( )
|
| A. | 乙烯、乙醇、乙醛 | B. | 乙炔、乙醛、乙二醇 |
|
| C. | 甲烷、甲醇、乙酸 | D. | 甲烷、甲酸甲酯、丙二酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是()
A. 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性
B. 等物质的量浓度的醋酸与醋酸钠溶液中水电离产生的c(OH﹣).前者小于后者
C. 沉淀溶解达到平衡时,溶液中溶质的离子浓度不一定相等,但保持不变
D. 水的离子积只与温度有关,向水中加入酸、碱或盐一定会影响水的电离平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
0.2mol有机物和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H20(气),产物通过浓硫酸,浓硫酸质量增加10.8g;再通过灼热CuO,充分反应后,CuO质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g.
(1)试推断该有机物的分子式.
(2)若0.2mol该有机物恰好与9.2g金属钠完全反应,试确定该有机物的结构简式并命名.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com